Autophagy-Lysosomal Pathway เป็นเป้าหมายการรักษาที่มีศักยภาพในโรคพาร์กินสัน
Jun 28, 2022
โปรดติดต่อoscar.xiao@wecistanche.comสำหรับข้อมูลเพิ่มเติม
เชิงนามธรรม:ระบบควบคุมคุณภาพเซลลูลาร์ได้รับความสนใจอย่างมากในทศวรรษที่ผ่านมา ในบรรดาสิ่งเหล่านี้ autophagy เป็นกลไกการรักษาตัวเองตามธรรมชาติที่กำจัดส่วนประกอบของเซลล์ที่เป็นพิษอย่างต่อเนื่องและทำหน้าที่เป็นกระบวนการต่อต้านริ้วรอย มันเป็นสิ่งสำคัญสำหรับการอยู่รอดของเซลล์และเพื่อรักษาสภาวะสมดุล มีการรายงานเส้นทาง autophagy ที่ขึ้นกับประเภทเซลล์หรือที่ไม่ใช่ Canonical ซึ่งแสดงระดับการเลือกที่แตกต่างกันโดยคำนึงถึงซับสเตรตที่เป็นเป้าหมาย ในที่นี้ เราขอนำเสนอการทบทวนกลไก autophagy ฉบับปรับปรุงและหารือเกี่ยวกับบทบาทของ autophagy รูปแบบต่างๆ ในโรคทางระบบประสาท โดยเน้นที่โรคพาร์กินสันโดยเฉพาะ เราอธิบายการค้นพบล่าสุดที่นำไปสู่ข้อเสนอของกลยุทธ์การรักษาที่กำหนดเป้าหมาย autophagy เพื่อเปลี่ยนเส้นทางของความก้าวหน้าของโรคพาร์กินสัน
คำสำคัญ:autophagy; ไลโซโซม; โรคทางระบบประสาท โรคพาร์กินสัน; ภูมิต้านทานตนเอง

กรุณาคลิกที่นี่เพื่อทราบข้อมูลเพิ่มเติม
1. บทนำ
แม้ว่าองค์ประกอบบางอย่างของโรคพาร์กินสัน (PD) จะได้รับการอธิบายไว้นานแล้ว แต่คำอธิบายทางการแพทย์ที่ชัดเจนครั้งแรกของโรคนี้ได้รับการตีพิมพ์ในปี พ.ศ. 2360 โดย James Parkinson [1] ตั้งแต่นั้นมา ได้มีการพยายามอย่างมากในการทำความเข้าใจเกี่ยวกับกลไกการเกิดโรคและองค์ประกอบทางพยาธิวิทยาของโรคที่ซับซ้อนนี้ ในแง่ของการเปลี่ยนแปลงทางระบบประสาทและทางกายวิภาค [2-5] PD เป็นโรคที่มีหลายปัจจัยซึ่งมีปัจจัยเชิงสาเหตุต่างกัน รวมถึงองค์ประกอบทางพันธุกรรม สิ่งแวดล้อม โมเลกุลและเซลล์ PD มีลักษณะอาการและอาการแสดงของมอเตอร์และไม่ใช่มอเตอร์ในวงกว้าง อาการเหล่านี้รวมถึงอาการสั่นขณะพัก, bradykinesia, ท่าเดินไม่มั่นคง/เดินไม่มั่นคง และความแข็งแกร่ง ควบคู่ไปกับความผิดปกติทางจิตเวช ความผิดปกติของการนอนหลับ สัญญาณของมอเตอร์เป็นผลมาจากการสูญเสียเซลล์ประสาทโดปามีนเนอร์จิก (DA) ใน substantia nigra pars compacta (SNpc) และการรวมภายในเซลล์ของ -synuclein(c-syn) ที่รวมตัวกันและพับผิด (c-syn) ที่ห่อหุ้มหรือไม่อยู่ใน Lewy body (LB) และ Lewy neurites ( LN) ในเซลล์ประสาท[3,6] (รูปที่ 1; ดูคำจำกัดความในภาคผนวก)
อาการของ PD จะค่อยๆ ขึ้นตามอายุcistanche คืออะไรพวกเขาสามารถเริ่มต้นด้วยการสั่นเล็กน้อยในมือข้างหนึ่งและความรู้สึกตึงในร่างกาย bradykinesia เป็นประจำ การศึกษาล่าสุดยืนยันว่ามากกว่า 3 เปอร์เซ็นต์ของประชากรทั่วไปอายุ 65 ปีได้รับผลกระทบจาก PD อย่างไรก็ตาม ใน 5 เปอร์เซ็นต์ -10 เปอร์เซ็นต์ของกรณี อาการของ PD ปรากฏขึ้นก่อนหน้านี้ สิ่งนี้เรียกว่า PD ที่เริ่มมีอาการวัยเยาว์ (YOPD) ผู้ชายมีแนวโน้มที่จะพัฒนา PD มากกว่าผู้หญิง 50 เปอร์เซ็นต์ แต่ความเสี่ยงสำหรับผู้หญิงดูเหมือนจะเพิ่มขึ้นตามอายุ

รูปที่ 1 ผลการตรวจทางระบบประสาทในโรคพาร์กินสัน (A, B) เยื่อหุ้มสมองอักเสบภายหลังการชันสูตรพลิกศพและ pons จากผู้ป่วยกลุ่มควบคุม (A) และจากผู้ป่วยที่มี PD(B): SN มีสีซีดกว่าใน B เนื่องจากการเสื่อมของ dopaminergic (C), SN, การย้อมสี H&E (×250).(D): การย้อมสี H&E (×250)ของ LB ในเซลล์ประสาทเยื่อหุ้มสมอง ลูกศรสีดำแสดง LB ตัวย่อที่ไม่ได้อธิบายไว้ในข้อความ: H&E, hematoxylin และ eosin
สาเหตุหลักของ PD ยังไม่เป็นที่ทราบแน่ชัดไบโอฟลาโวนอยด์บางกรณีของ PD มีความเชื่อมโยงกับการกลายพันธุ์ทางพันธุกรรม แต่สาเหตุทางพันธุกรรมที่ชัดเจนของโรคนี้ยากที่จะสร้าง แท้จริงแล้วมีเพียง 15 เปอร์เซ็นต์ของผู้ป่วยที่เป็น PD เท่านั้นที่มีประวัติครอบครัวเป็นโรคนี้ ยีนบางตัวมีความเกี่ยวข้องกับรูปแบบของโรคที่ชัดเจน เป็นธรรมดา หรือหายากกว่า ซึ่งรวมถึงรูปแบบที่เด็กหรือผู้ใหญ่เริ่มมีอาการในช่วงต้นหรือปลาย ภาวะถอยกลับอัตโนมัติ ลักษณะเด่น หรือรูปแบบ X-linked [4,7-9] นอกจากนี้ยังระบุปัจจัยเสี่ยงเชิงสาเหตุที่เกี่ยวข้องกับกลุ่มชาติพันธุ์เฉพาะอีกด้วย ยีนที่เชื่อมโยงกับ PD บ่อยที่สุด ได้แก่ GBA, LRRK2, PRKN, SNCA, ATP13A2, ATP10B, DI-1,DNAIC6, FBXO7,HTRA2,MAPT, PINK1,PLA2G6,VPS35,และ VPS13C[4,{{19} }]. ยีนเหล่านี้ส่วนใหญ่เข้ารหัสโปรตีนที่เชื่อมโยงโดยตรงหรือโดยอ้อมกับกลไกการควบคุมคุณภาพที่มีความสำคัญในการรักษาสภาวะสมดุลของเซลล์ เส้นทางการขนส่งของตุ่ม กระบวนการ autophagy และระบบ endo-lysosomal การเปลี่ยนแปลงทางพันธุกรรมอื่นๆ ยังเกี่ยวข้องกับ PD รวมถึงการเปลี่ยนแปลงของอีพีเจเนติก เช่น DNA methylation, chromatin remodeling, histone modified, microRNAs และ long non-coding RNAs [4,14]
2. การเกิดโรคและพยาธิวิทยา
การศึกษาทางคลินิกทางพยาธิวิทยาเผยให้เห็นความก้าวหน้าช้าของ PD จากบริเวณ ventrolateral ของ SNpc และแพร่กระจายไปยังบริเวณสมองอื่น ๆ ในภายหลัง [15] อาการทางคลินิกของ PD จะตรวจพบได้เมื่อความเสื่อมของเซลล์ประสาท DA ดำเนินไปภายใน SNpc พบ LBs ที่บริเวณที่เกิดความเสียหายต่อเซลล์ประสาท (รูปที่ 1) ในสรีรวิทยาปกติ -syn ที่ฝากไว้ในโครงสร้างเหล่านี้ทำหน้าที่ศูนย์กลางในเอนโดไซโทซิส การค้าถุงอัณฑะ; การสังเคราะห์ การเก็บรักษา และการปล่อยโดปามีน Ca2 บวกกับสภาวะสมดุล; ไดนามิกของไมโครทูบูล และกระบวนการอื่นๆ [16] ดังนั้นกิจกรรมของเซลล์ประสาทจึงขึ้นอยู่กับ -syn และสภาวะสมดุลของยล แม้ว่า -syn จะปรากฏเด่นชัดใน LBs ของ cytosolic eosinophilic แต่ก็ยังตรวจพบใน mitochondria, lysosomes และ organelles อื่น ๆ ในสมอง PD ภายหลังการชันสูตรพลิกศพ การปรากฏตัวของ LBs ในระบบประสาทส่วนปลาย ลำไส้ และส่วนกลาง (CNS) มีส่วนเกี่ยวข้องกับอาการของ PD ทั้งจากมอเตอร์และไม่ใช่มอเตอร์ [17,18]ซื้อ cistancheการกลายพันธุ์ของจุดในลำดับ -syn หรือการดูถูกทางพยาธิวิทยาอื่นๆ นำไปสู่การก่อตัวของโอลิโกเมอร์ ซึ่งอาจรวมกลุ่มเข้าด้วยกันเป็นกลุ่มที่ใหญ่ขึ้น การรวมกลุ่มเหล่านี้สามารถเปลี่ยนแปลงวิถีของเซลล์และโมเลกุลในเซลล์ประสาทได้มากมาย โดยเฉพาะอย่างยิ่งที่เกี่ยวข้องกับกระบวนการ autophagy และ proteasomal เช่น หน้าที่ของไมโตคอนเดรีย การค้าถุงอัณฑะ ออร์แกเนลล์ และการเสื่อมสภาพของโปรตีน ซึ่งทั้งหมดนี้นำไปสู่การเสื่อมของระบบประสาท ต่อมา จากการเสื่อมสภาพของระบบประสาท มวลรวมของ o-syn จะถูกสะสมใน SN โดยที่พวกมันกระตุ้น microglia [19] การกระตุ้นที่ไม่สามารถควบคุมได้นี้สามารถสร้างสัญญาณที่ทำให้เกิดการอักเสบได้ [20] ซึ่งอาจนำไปสู่การเสื่อมของระบบประสาทอีกเมื่อถึงเกณฑ์วิกฤต

Cistanche สามารถต่อต้านริ้วรอย
2.1.อาการทางระบบประสาทของ PD
ไม่มีการทดสอบเฉพาะเพื่อวินิจฉัย PD ดังนั้น การวินิจฉัยจะขึ้นอยู่กับประวัติทางการแพทย์ การทบทวนอาการ และการตรวจระบบประสาทและร่างกาย (Box1) อาการแสดงของ PD มักจะเริ่มเมื่ออายุประมาณ 60 ปี [21] แต่ YOPD ไม่ได้เกิดขึ้นบ่อยนัก โดยเฉพาะอย่างยิ่งในรูปแบบทางพันธุกรรมบางอย่าง [22] bradykinesia ข้างเดียวหรือไม่สมมาตรและ / หรือแรงสั่นสะเทือนที่เหลือเป็นอาการแรกของโรค [23] อาการสั่นขณะพักมีอยู่ในกล้ามเนื้อที่ผ่อนคลายและหายไประหว่างการเคลื่อนไหวและการนอนหลับ อาจเพิ่มขึ้นด้วยการคำนวณทางจิต Bradykinesia กำหนดโดยความช้าของการเคลื่อนไหวและแอมพลิจูดหรือความเร็วที่ลดลง นำไปสู่ความยากลำบากในการเคลื่อนไหวซ้ำๆ, micrography, การเดินก้าวเล็ก ๆ และความยากลำบากในการพูด (hypophonia และ dysarthria) ซึ่งจะเกิดขึ้นเมื่อโรคมีวิวัฒนาการcistanchความแข็งอาจทำให้เกิดอาการปวดและส่งผลต่อการทรงตัว (งอกระดูกสันหลังส่วนทรวงอก) ความก้าวหน้าช้าด้วยการขยายทวิภาคีของ akinesia, tremor และ hypertonia ตามมาด้วยความไม่มั่นคงของท่าทาง, การแช่แข็งของการเดิน, การหกล้มและในผู้ป่วยบางราย Camptocormia สัญญาณที่ไม่ใช่มอเตอร์ (premotor) อาจเกิดขึ้นหลายปีก่อนอาการของมอเตอร์ครั้งแรก เหล่านี้รวมถึงภาวะซึมเศร้า, ภาวะน้ำตาลในเลือดต่ำ, ท้องผูก, หรือความผิดปกติของการนอนหลับที่เคลื่อนไหวเร็ว [24] อาจมีความวิตกกังวลและความเฉื่อยชาตั้งแต่เริ่มมีอาการของ PD ในขณะที่ dysautonomia รุนแรง (orthostatic hypotension, ความผิดปกติของระบบปัสสาวะเนื่องจาก detrusor hyperactivity), การกระจายตัวของการนอนหลับ, ความผิดปกติทางการรับรู้ (ความผิดปกติ dysexecutive) และอาการประสาทหลอนเกิดขึ้นในภายหลังและจะส่งผลให้สูญเสียเอกราช [ 24,25].

2.2. การรักษาปัจจุบันสำหรับ PD และการจัดการทางคลินิก
การรักษาตามอาการเป็นทางเลือกเดียวที่มีอยู่ในปัจจุบัน [26] โดยมีการรักษาเพื่อชดเชยการขาดสารโดปามีน ยาโดปามีนเนอร์จิก(levodopa ที่เกี่ยวข้องกับตัวยับยั้ง dopa-decarboxylase, ตัวเร่งปฏิกิริยา dopaminergic หรือสารยับยั้ง monoamine oxidase-type B) ใช้เดี่ยวหรือในสูตรการรักษาแบบโพลีบำบัดนั้นมีประสิทธิภาพมากในช่วงแรกของโรค อย่างไรก็ตาม การจัดการจะยากขึ้นตามความก้าวหน้าของปี อันที่จริง การรักษาด้วยโดปามีนซึ่งปรับปรุงสัญญาณของการเคลื่อนไหว อาจมีภาวะแทรกซ้อนที่ทุพพลภาพอย่างมาก ปรากฏการณ์การเสื่อมสภาพ (การสิ้นสุดของปริมาณยาล้มเหลว) และอาการดายสกินเกิดขึ้นหลังจากการรักษาเลโวโดปาเป็นเวลาหลายปี [27] ความผิดปกติของการควบคุมแรงกระตุ้น (การเล่นการพนันทางพยาธิวิทยาหรือการช้อปปิ้ง การมีเพศสัมพันธ์มากเกินไป [28] ภาพหลอนหรือโรคจิตอาจทำให้การรักษาโดปามีนที่ซับซ้อน และมักพบร่วมกับตัวเร่งปฏิกิริยาโดปามีน [29] การรักษาอื่น ๆ รวมทั้งสารยับยั้ง catechol-O-methyltransferase ของ apomorphine, การให้ droxidopa gel อย่างต่อเนื่อง, การกระตุ้นด้วยนิวเคลียร์ subthalamic ทวิภาคี) เมื่อความผันผวนของมอเตอร์และดายสกินมีความสำคัญ [30] การรักษาเหล่านี้มีจุดมุ่งหมายเพื่อให้เกิดการกระตุ้นโดปามีนใน striatal ที่เสถียร แต่ไม่มีผลกระทบต่อการลุกลามของโรค นอกจากนี้ อาการทางแกนบางอย่าง (dysarthria, postural instability) ไม่ไวต่อสาร dopa และการจัดการทางคลินิกของ non-motor อาการยังคงยาก [31,32].
การวิจัยหลายทศวรรษได้นำไปสู่การพัฒนากลยุทธ์การรักษา ซึ่งทำให้คุณภาพชีวิตของผู้ป่วยดีขึ้นอย่างไม่ต้องสงสัย อย่างไรก็ตาม การชะลอการลุกลามของโรคยังคงเป็นเรื่องท้าทาย และยังคงให้ความสำคัญอย่างต่อเนื่อง [33] และแนวทางใหม่ในการปรับเปลี่ยนโรคต่างรอคอยอย่างใจจดใจจ่อ [3,34] แม้ว่าหน้าที่ของโปรตีอาโซมและออโตฟาจี ซึ่งรวมถึงมาโครออโตฟาจีและออโตฟาจีที่มีพี่เลี้ยงเป็นสื่อกลาง (chaperone-mediated autophagy (CMA)) เป็นที่ทราบกันมานานแล้วว่ามีส่วนในการกวาดล้าง -syn กวาดล้าง [35,36l การควบคุมการผิดปกติของกระบวนการเหล่านี้ยังคงไม่ค่อยเข้าใจใน PDcistanche ออสเตรเลียการกลายพันธุ์และการดัดแปลงของยีนหลายอย่างที่เกี่ยวข้องกับ PD มีการเชื่อมโยงอย่างใกล้ชิดกับ autophagy โดยเฉพาะอย่างยิ่ง mitophagy และวิถี autophagy-lysosomal ในการทบทวนนี้ เราเน้นที่การมีส่วนร่วมของ autophagy ใน PD แสดงความคิดเห็นเกี่ยวกับคำถามที่ยังไม่ได้ตอบที่สำคัญในฟิลด์ และเสนอแนวทางใหม่สำหรับการรักษาที่เป็นไปได้ซึ่งกำหนดเป้าหมายเส้นทาง autophagy
3. ออโตฟาจี
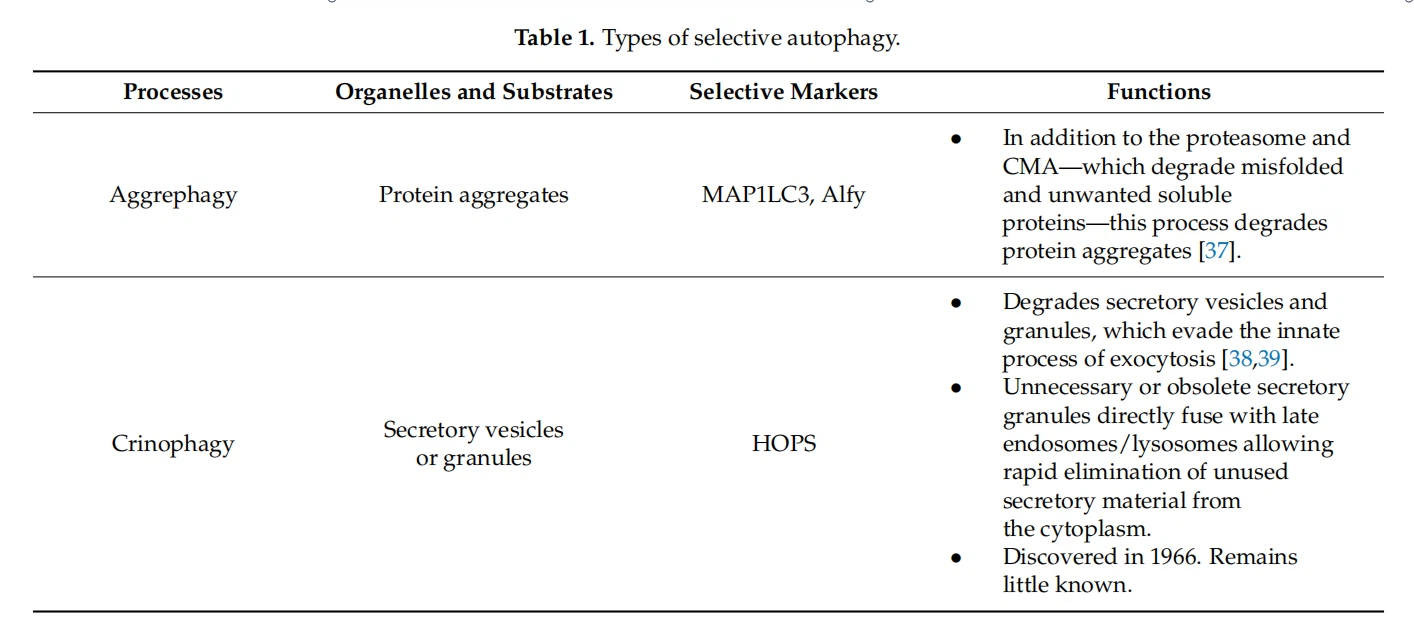
Autophagy เป็นระบบการย่อยสลายภายในเซลล์ที่สำคัญโดยที่วัสดุไซโตพลาสซึมถูกส่งไปยังไลโซโซมเพื่อการย่อยสลาย ตามเส้นทางที่เนื้อหาถูกส่งไปยังไลโซโซม มีการกำหนด autophagy หลายรูปแบบ รูปแบบที่แตกต่างกันเหล่านี้ยังมีระดับการเลือกที่แตกต่างกันสำหรับสินค้าเป้าหมาย (ตารางที่ 1; รูปที่ 2) กระบวนการ autophagy หลักสามประเภท ได้แก่ macroautophagy, CMA และ microautophagy/EMI ไม่ว่าเส้นทางการจัดส่งจะเป็นอย่างไร บทบาทหลักของกระบวนการเหล่านี้คือการย่อยสลายวัสดุที่ไม่ต้องการซึ่งมีข้อบกพร่อง อาจเป็นพิษ หรือมีการผลิตมากเกินไป และเพื่อรักษาสภาวะสมดุลของเซลล์
3.1.เครื่องจักรอัตโนมัติ
กลไกของ autophagy ได้รับการตรวจสอบอย่างละเอียดและได้รับการตรวจสอบอย่างละเอียดโดยผู้เขียนหลายคน [61-63] ลักษณะทั่วไปของเส้นทางทั้งสามแสดงไว้ในรูปที่ 2 ความก้าวหน้าล่าสุดที่เกี่ยวข้องกับกระบวนการ autophagic ที่เป็นที่ยอมรับและไม่ใช่ Canonical โดยเฉพาะอย่างยิ่งในระบบของสัตว์เลี้ยงลูกด้วยนมได้เพิ่มความเข้าใจของเราเกี่ยวกับกลไกที่อาจมีบทบาทสำคัญในโรคทางระบบประสาทเช่น PD อย่างไรก็ตาม การค้นพบโมเลกุลหลายอย่างที่ความเข้าใจในปัจจุบันของเราเกี่ยวกับการควบคุม autophagy เกิดขึ้นจากการวิเคราะห์ที่เกี่ยวข้องกับยีสต์ ในเซลล์ autophagy ทั้งสามรูปแบบจะอยู่ร่วมกันและมีบทบาทสำคัญในการรักษาสภาวะสมดุลของเซลล์ อย่างไรก็ตาม ผลลัพธ์ส่วนใหญ่ที่มีอยู่ในฟิลด์นี้เกี่ยวข้องกับ macroautophagy กระบวนการนี้แบ่งออกเป็นขั้นตอนต่อไปนี้: นิวเคลียส การยืดตัว การก่อรูปออโตฟาโกโซม การหลอมรวมออโตฟาโกโซม-ไลโซโซม และการเสื่อมสภาพ (รูปที่ 2) แต่ละขั้นตอนมีการควบคุมทางพันธุกรรมอย่างประณีตและมีบทบาทเฉพาะของตนเองในการรักษาธรรมชาติแบบไดนามิกของกระบวนการ ตัวอย่างเช่น โปรตีนที่เกี่ยวข้องกับ autophagy ที่อนุรักษ์ไว้จำนวนหนึ่งทำหน้าที่ในลักษณะลำดับชั้นเพื่อไกล่เกลี่ยการก่อรูปออโตฟาโกโซม เมื่อเหนี่ยวนำต้นน้ำ เครื่องจักร autophagy จะสัมผัสกับเมมเบรนแยก/phagophore ต้นกำเนิดในระยะเริ่มต้นและเอนโดพลาสมิก เรติคูลัม (ER) แหล่งกำเนิดที่ซับซ้อนขั้นสุดท้าย (ER) กอลจิคอมเพล็กซ์ เอนโดโซม และไมโทคอนเดรีย] ของเยื่อหุ้มการแยกตัวตั้งไข่ยังคงเป็นประเด็นถกเถียง [64] การศึกษาโครงสร้างพื้นฐานที่เกี่ยวข้องกับการทดลองด้วยกล้องจุลทรรศน์อิเล็กตรอนยืนยันว่าโดเมนย่อยเฉพาะของ ER มีส่วนช่วยในการสร้าง phagophore [65] โปรตีนที่เกี่ยวข้องกับ autophagy (ATG) ประมาณ 40 ตัวได้รับการระบุว่าเกี่ยวข้องกับกระบวนการไดนามิกนี้ พวกมันถูกจัดระเบียบตามลำดับชั้น เริ่มจากการเริ่มต้นของกระบวนการและดำเนินไปจนถึงการเจริญเติบโตของออโตฟาโกโซม โปรตีนเหล่านี้ทำงานร่วมกันในสารเชิงซ้อนเชิงฟังก์ชันหลายอย่าง โดยเฉพาะอย่างยิ่ง (i) Unc-51-like kinase 1(ULK1)/ATG1 kinase complex; (ii) คลาส II phosphatidylinositol (PI)3-kinase complex;(ii) PI(3)P-binding ATG2-ATG18 complex;(iv)ทั้งสองระบบคอนจูเกต (ระบบการคอนจูเกต ATG12 และ โปรตีนที่เกี่ยวข้องกับไมโครทูบูล 1A/1B-สายเบา 3(MAP1LC3)/ระบบคอนจูเกต ATG8); และ (v) เครื่องจักรหลอมรวม (รูปที่ 2)

อันที่จริง โปรตีน ATG หลายตัวที่เรียกว่ามีฟังก์ชันทางเลือกอื่นนอกเหนือจาก autophagy [66] ดังนั้น ตัวอย่างเช่น การลิปิดของ MAP1LC3 (กลไกที่ใช้มานานแล้วในการประเมินการออกฤทธิ์ของ autophagic [67,68]) ยังเกี่ยวข้องกับกลไกของเซลล์ที่ไม่ใช่ autophagic เช่น phagocytosis, LAP, micropinocytosis หรือการติดเชื้อไวรัส กระบวนการเหล่านี้เรียกว่ากระบวนการ autophagic ที่ไม่เป็นที่ยอมรับ [69] ในกระบวนการที่ไม่เป็นไปตามรูปแบบบัญญัติเหล่านี้ หน้าที่ซึ่งยังคงแสดงคุณลักษณะที่ไม่สมบูรณ์ [70,71] MAP1LC3 คอนจูเกตกับเยื่อหุ้มเซลล์เดียว (การคอนจูเกต ATG8 ของเมมเบรนเดียว, SMAC) และองค์ประกอบไซโตซอลไม่ถูกส่งไปยังไลโซโซม [72]
3.2. Autophagy ของเส้นประสาทมีส่วนทำให้เกิดสรีรวิทยาของเส้นประสาท
มีหลักฐานที่น่าสนใจที่สนับสนุนแนวคิดที่ว่า autophagy ของเซลล์ประสาทมีบทบาทชี้ขาดในหลาย ๆ ด้านของการพัฒนาเซลล์ประสาทและในการรักษากิจกรรมของเซลล์ประสาท [73-75] ในเซลล์หลังไมโทซิส เช่น เซลล์ประสาท การ autophagy มีความสำคัญอย่างยิ่งต่อการอยู่รอดและสภาวะสมดุล เนื่องจากเซลล์เหล่านี้ไม่สามารถกำจัดสารพิษที่สะสมและออร์แกเนลล์ที่เสียหายระหว่างการแบ่งเซลล์ได้ Autophagy เช่นเดียวกับระบบ proteasomal [76] จึงเป็นหนึ่งในกลไกการควบคุมคุณภาพที่สำคัญที่ช่วยให้เซลล์ประสาทมีอายุยืนยาว การ autophagy แบบพรีไซแนปติกในเทอร์มินัลแอกซอนก็มีความจำเป็นสำหรับการบำรุงรักษาซินแนปติกและความเป็นพลาสติกเช่นกัน [77]
ในบรรดาเซลล์ประสาท มีเพียงเซลล์ประสาทคอร์เทกซ์ เซลล์ Purkinje และเซลล์ประสาทไฮโปทาลามิคเท่านั้นที่สามารถเพิ่มเนื้อหาออโตฟาโกโซมของพวกมันเมื่อถูกกระตุ้น สาเหตุที่แน่ชัดสำหรับกลไกเฉพาะนี้ยังไม่ทราบ [62,78] คำอธิบายที่เป็นไปได้ประการหนึ่งเป็นเรื่องเล็กน้อยและเกี่ยวข้องกับความจริงที่ว่า เช่นเดียวกับเซลล์ประเภทอื่นๆ การวัด autophagy ในเซลล์ประสาท โดยเฉพาะอย่างยิ่งในสมอง ยังคงมีความท้าทาย [79,80] อีกทางหนึ่ง เนื่องจากเซลล์ประสาทมีความแตกต่างในระยะสุดท้าย ด้วยความสามารถในการสร้างใหม่ต่ำกว่าเซลล์อื่นๆ พวกมันจึงมี autophagic น้อยกว่า อย่างไรก็ตาม การศึกษาเกี่ยวกับสมองจากหนูที่ขาด autophagy ได้ให้หลักฐานว่าโปรตีน sequestosome-1 (SQSTM1)/p62 และโปรตีน polyubiquitinated สะสมในเซลล์ประสาทส่วนใหญ่[81] ในทางตรงกันข้าม การขาด SQSTM1 ไม่ได้ส่งผลให้ขาด autophagy อย่างสมบูรณ์ ดังนั้นดูเหมือนว่าเนื้อหา autophagosome จะขึ้นอยู่กับชนิดของเซลล์และชนิดของตัวสร้างความเครียด
3.3. Autophagy และโรคทางระบบประสาท
ตามที่แนะนำข้างต้น เพื่อป้องกันความผิดปกติของเซลล์ประสาทและไซแนปติก เซลล์ประสาทได้พัฒนากลไกเพื่อกำจัดส่วนประกอบและออร์แกเนลล์ที่เป็นพิษและบกพร่อง กลไกเหล่านี้จำเป็นต่อการรักษาระดับของสารสื่อประสาทและความสมบูรณ์ของโปรตีโอมที่ทำงานในเซลล์ประสาท Autophagy เป็นศูนย์กลางของระบบป้องกันนี้ การสูญเสียการทำงานของ autophagy ที่เกี่ยวข้องกับอายุทำให้เซลล์ประสาทมีความเสี่ยงต่อความเครียดมากขึ้นและอาจทำให้เซลล์ตายได้ [82] การหยุดชะงักทางพยาธิวิทยาของวิถี autophagy อาจส่งผลให้เกิดความผิดปกติของระบบประสาทที่อาจหรือไม่อาจเชื่อมโยงกับความชรา
autophagy ที่ถูกทำลายได้รับการบันทึกไว้ในโรคเกี่ยวกับระบบประสาทหลายชนิด รวมทั้ง PD, โรคอัลไซเมอร์ (AD), โรคฮันติงตัน (HD) และเส้นโลหิตตีบด้านข้าง amyotrophic (ALS) (สำหรับการทบทวนอย่างครอบคลุม ดู [63.84]) การตรวจสอบกลไกที่เชื่อมโยง autophagy กับโรคเหล่านี้ มีการสังเกตพบ เช่น หนูที่ขาด Atg5 ในเซลล์ประสาทโดยเฉพาะจะพัฒนาความบกพร่องในการทำงานของมอเตอร์ในขณะที่ยังสะสมตัวรวมของไซโตพลาสซึมในเซลล์ประสาทด้วย[85] ในทำนองเดียวกัน ในหนูที่ขาด Atg7, Atg5 หรือ Ambral พบว่า ubiquitin สะสมใน CNS และการรวมตัวของไซโตพลาสซึมเกี่ยวข้องกับความผิดปกติของมอเตอร์ และข้อบกพร่องของหลอดประสาทในตัวอ่อนของหนู [86] การกลายพันธุ์ของยีนที่เชื่อมโยงกับกระบวนการ autophagic—เช่น SQSTM1, optineurin/OPTN, E3 ubiquitin ligase PARKIN/PRKN, PINK1, TBK1— มีส่วนเกี่ยวข้องในโรคทางระบบประสาทหลายชนิดเช่นกัน โดยเฉพาะอย่างยิ่ง ข้อบกพร่องใน mitophagy ที่พบในโรคเกี่ยวกับอวัยวะเฉพาะและการอักเสบของระบบได้รับการบันทึกไว้ในโรคเกี่ยวกับระบบประสาท [87] นอกเหนือจากการกลายพันธุ์ทางพันธุกรรมเหล่านี้ การเปลี่ยนแปลงที่สำคัญในการแสดงออกของโปรตีนยังเชื่อมโยงกับโรคทางระบบประสาทอีกด้วย ตัวอย่างเช่น การแสดงออกที่ผิดปกติของเซลล์เยื่อบุผิวต่อมโปรตีน 1 (GABARAPL1/GEC1) เกี่ยวข้องกับโรคทางระบบประสาท [88] 3.4. Autophagy และโรคพาร์กินสัน
ในบรรดาลักษณะเด่นทางพยาธิวิทยาของ PD คือ LB ที่มีโปรตีน -syn รวมอย่างผิดปกติ การกลายพันธุ์หรือสามเท่าของการเข้ารหัสยีน -syn (SNCA) นั้นหายาก แต่เกี่ยวข้องอย่างชัดเจนในการเริ่มต้นและความก้าวหน้าของ PD ที่น่าสนใจคือ ความล้มเหลวใดๆ ที่ส่งผลกระทบต่อส่วนประกอบหนึ่งของกระบวนการย่อยสลาย ไม่ว่าทางตรงหรือทางอ้อม จะบั่นทอนกระบวนการ autophagy อื่นๆ ระบบ ubiquitin-proteasome (UPS) เป็นที่ทราบกันดีว่าเป็นวิถีการย่อยสลายหลักสำหรับ monoubiquitinated -syn ในขณะที่วิถีทาง macroautophagy จะลดระดับ deubiquitinated a-syn [89,90] ใน PD ดังนั้น ทั้งไมโตคอนเดรียและไลโซโซมจึงมีบทบาทสำคัญ (รูปที่ 3) 3.4.1.บทบาทของ Mitophagy ใน PD
ในฐานะที่เป็นออร์แกเนลล์ที่สร้างพลังงาน ไมโทคอนเดรียนเป็นศูนย์กลางของโรคทางระบบประสาทหลายอย่าง รวมถึง PD [91-95] การตรวจสอบหลายครั้งพบว่าการกลายพันธุ์ทางพันธุกรรมที่เกี่ยวข้องกับ PD (เช่น PRKN, PINK1 และอื่นๆ) ยังเชื่อมโยงอย่างใกล้ชิดกับข้อบกพร่องของไมโตคอนเดรีย ซึ่งรวมถึงข้อบกพร่องในไมโทฟาจี (ตารางที่ 2)[9] ประเภทของความเสียหายที่เกิดกับไมโทคอนเดรียนั้นขึ้นอยู่กับชนิดของ a-syn (การก่อตัวเป็นมวลรวมหรือไม่เกิดขึ้นจาก SNCA ที่กลายพันธุ์หรือโดยกำเนิด) การศึกษาเพิ่มเติมยืนยันว่า o-syn ส่งผลต่อปฏิสัมพันธ์ของเยื่อหุ้มเซลล์ที่เกี่ยวข้องกับไมโตคอนเดรียกับ ER ปฏิสัมพันธ์นี้มีบทบาทสำคัญในการควบคุม Ca4 บวกกับการส่งสัญญาณและการตายของเซลล์ นอกจากนี้ o-syn ที่ผิดปกติรบกวนการทำงานของ peroxisome proliferator-activated receptor-gamma coactivator 1-alpha ซึ่งมีบทบาทสำคัญในการสร้าง mitochondrial biogenesis และ apoptosis ความผิดปกติของไมโตคอนเดรียกับการมีส่วนร่วมของปัจจัยที่เกี่ยวข้องกับ a-syn ได้รับการกล่าวถึงอย่างครอบคลุมในที่อื่น [9,97,98]

รูปที่ 3 การด้อยค่าของ autophagy ใน PD มีการสังเกตรูปแบบ autophagy ที่บกพร่องใน PD การกลายพันธุ์ทางพันธุกรรมของ -syn เชื่อมโยงกับการด้อยค่าของกระบวนการ autophagy ปัจจัยหลายอย่าง เช่น ปัจจัยทางพันธุกรรม การค้าไมโตคอนเดรียที่บกพร่อง ความเครียดจากปฏิกิริยาออกซิเดชัน วัฏจักร ATP ที่ผิดปกติ การเปลี่ยนแปลงของไมโตคอนเดรียที่ถูกควบคุม และการสร้างไมโตคอนเดรียที่เปลี่ยนแปลงไปทำให้ไมโตคอนเดรียมีสุขภาพดี ไมโตคอนเดรียที่เสียหาย/ทำงานผิดปกติทำให้ PINK1 สามารถคัดเลือก PRKN ซึ่งจะกระตุ้นโปรตีนที่จำเป็นอื่นๆ เช่น OPTN และ ubiquitin, Rab7 และอื่นๆ จึงเป็นการเริ่มต้นกระบวนการควบคุมคุณภาพ กล่าวคือ ไมโทฟาจี ฟังก์ชันของ Rab7 ถูกควบคุมโดย TBC1D15/17 (เป็นของตระกูล TBC ที่มีฟังก์ชัน Rab-GAP) ซึ่งควบคุมฟังก์ชันการขึ้นรูปและเป้าหมายของเมมเบรนการแยกด้วยการเชื่อมโยงข้ามกับ Fis1 และ MAP1LC3B ขั้นตอนที่ต่อเนื่องกันของไมโทฟาจีคือการก่อตัวของฟาโกฟอร์ การเจริญเต็มที่ในไมโตออโตฟาโกโซม และการรวมตัวของไมโตออโตฟาโกโซมกับไลโซโซม autophagy แบบธรรมดายังมีบทบาทสำคัญในการย่อยสลาย -syn (ทั้งแบบไร้เดียงสาและแบบรวม) x-syn เลือกจับกับตัวรับการรู้จำเชื้อโรค TLR-4 ซึ่งกระตุ้นเส้นทางการส่งสัญญาณดาวน์สตรีมหลังการกระตุ้น NF-kB เพื่อกระตุ้นการผลิต SQSTM1/p62 SQSTM1 ที่สร้างขึ้นจะผูกกับ internalized -syn และเริ่มกระบวนการ autophagy ความผิดปกติของกระบวนการ autophagy นำไปสู่การสะสมของ -syn ควบคู่ไปกับ SQSTM1 นอกเหนือจาก mitophagy และ macroautophagy แล้ว CMA ยังเลือกลดระดับ -syn ซึ่งมี motif คล้าย KFERQ การยับยั้ง CMA แบบเลือกหรือการทำงานของ CMA ที่เปลี่ยนแปลงส่งผลต่อการย่อยสลาย -syn ตัวย่อที่ไม่ได้อธิบายไว้ในข้อความ: เติม ไมโตคอนเดรียฟิชชัน 1 โปรตีน; GAP, โปรตีนกระตุ้น GTPase; IKK, IkB ไคเนส; MyD88, โปรตีนสร้างความแตกต่างของมัยอีลอยด์ 88; Rab, Ras superfamily ของโปรตีน G ขนาดเล็ก; TBC, Tre-2/Bub2/Cdc16; TIRAP, โปรตีนอะแดปเตอร์ตัวรับ Toll-interleukin 1

ข้อบกพร่องในวิถี mitophagy โดยเฉพาะอย่างยิ่ง PARK2 (การกลายพันธุ์ PRKN) และ PARK6 (การกลายพันธุ์ PINK1) ได้รับการเสนอให้เป็นสาเหตุหลักของ PD ในครอบครัว ในสภาวะที่มีสุขภาพดี PINK1 ซึ่งแปลเป็นภาษาท้องถิ่นของไมโตคอนเดรีย จะถูกย้ายไปยังเยื่อหุ้มชั้นในของไมโตคอนเดรียซึ่งจะถูกย่อยสลาย ภายใต้สภาวะที่ไม่ทราบสาเหตุบางประการ ไมโทคอนเดรียจะเสียหายและสูญเสียศักยภาพของเมมเบรน (รูปที่ 3) สิ่งนี้นำไปสู่การกระตุ้น PINK1 และการจัดหา PRKN ซึ่งช่วยกระตุ้นการแบ่งเซลล์ในขณะที่ทำหน้าที่เกี่ยวกับโปรตีนเยื่อหุ้มไมโตคอนเดรียอื่นๆ OPTN และโปรตีนจุดนิวเคลียส 52-kDa (NDP52)][62,119-124] การกลายพันธุ์ของ PRKN เป็นสาเหตุที่พบบ่อยที่สุดของ YOPD แบบถอยอัตโนมัติ ตามด้วยการกลายพันธุ์ใน PINK1 นอกเหนือจากบทบาทในไมโทฟาจีแล้ว PRKN ยังมีบทบาทสำคัญในการประมวลผลไขมันและการแพร่หลายของ GTPase Rab7 ซึ่งควบคุมการเปลี่ยนแปลงของไลโซโซม [125-128] การขาด PRKN ส่งผลให้เกิดการเสื่อมของเซลล์ประสาท DA ในหนู และไฟโบรบลาสต์ของตัวอ่อนที่ได้มาจาก PINK1-หนูที่บกพร่องจะแสดงความผิดปกติของไลโซโซม [129] นอกจากนี้ การกลายพันธุ์ใน PINK1 และ PRKN ทำให้เกิดข้อบกพร่องในกระบวนการไมโทฟาจี [62] อย่างไรก็ตาม การศึกษายังไม่ได้อธิบายว่าทำไม PRKN จึงไม่คัดเลือกไมโตคอนเดรียในเซลล์ประสาท DA ภายใต้สภาวะขั้ว [130] ผลที่ตามมาของความผิดปกติของไมโทฟาจีในเซลล์ประสาทคือความเครียดที่ไม่สามารถควบคุมได้ (เช่น การสร้างออกซิเจนชนิดปฏิกิริยา) ซึ่งทำให้เซลล์ประสาทตายได้ สอดคล้องกับผลกระทบนี้ การกำหนดเป้าหมายข้อบกพร่องของ mitophagy อาจเป็นประโยชน์ใน PD ตัวอย่างเช่น มีการแสดงให้เห็นแล้วว่าตัวยับยั้งของ mitochondrial deubiquitinase USP30 ซึ่งควบคุม mitophagy ที่อาศัย PRKN ในเชิงลบ คัดเลือกเพิ่มฟลักซ์ของ mitophagy ดังนั้นจึงอาจเป็นที่สนใจสำหรับการพัฒนาวิธีการรักษาแบบใหม่ [131,132]
นอกจากผลกระทบที่สำคัญของการกลายพันธุ์ของ PINK1 และ PRKN แล้ว การกลายพันธุ์ของ SNCA ยังได้รับการศึกษาในบริบทของไมโทฟาจีอีกด้วย -syn ทำปฏิกิริยากับโปรตีน Miro (โปรตีนอะแดปเตอร์เยื่อหุ้มไมโตคอนเดรียชั้นนอก มีประโยชน์ในการเคลื่อนที่ของไมโตคอนเดรีย) และรบกวนกระบวนการย่อยสลายของไมโร ซึ่งเป็นขั้นตอนสำคัญในกระบวนการไมโทฟาจี[133] การศึกษาในหนูทดลองและการกลายพันธุ์ของยีสต์ที่เก็บอยู่ใน SCNA ยืนยันบทบาทของ -syn ในการตายของเซลล์ประสาท ผ่านทางความผิดปกติของไมโตคอนเดรีย [134,135]
ปัจจัยการถอดรหัส myocyte Enhancer factor 2D (MEF2D) เป็นอีกหนึ่งตัวควบคุมไมโตคอนเดรียที่จำเป็น (ตารางที่ 2) เป็นปัจจัยหลักในการส่งสัญญาณนอกเซลล์และกระตุ้นการทำงานของโปรแกรมทางพันธุกรรมเพื่อตอบสนองต่อสิ่งเร้าที่หลากหลายในเซลล์หลายประเภท รวมถึงเซลล์ประสาท MEF2D เป็นตัวควบคุมที่สำคัญของการแสดงออกของยีน IL-10 ที่เกี่ยวข้องกับการควบคุมเชิงลบของการตอบสนองต่อการอักเสบของ microglial และการป้องกันความเป็นพิษต่อเซลล์ที่เกิดจากการอักเสบ[136] MEF2Dexpression ที่ลดลงมีการเชื่อมโยงโดยตรงกับระดับที่ลดลงของ nicotinamide adenine dinucleotide dehydrogenase 6 (NADH) ซึ่งเป็นส่วนประกอบของ mitochondrial complex I การวิเคราะห์หลังชันสูตรศพของตัวอย่างสมองจากผู้ป่วย PD เผยให้เห็นระดับที่ลดลงของทั้ง MEF2D และ NADH [137]
การกลายพันธุ์ทางพันธุกรรมอื่นๆ จำนวนหนึ่ง ซึ่งรวมถึงข้อบกพร่องในปัจจัยกระตุ้นการตายของเซลล์ไมโตคอนเดรีย (AF) และปัจจัยการถอดรหัสของไมโตคอนเดรีย A (TFAM;[138] ที่รบกวนวิถีของเอนโด-ไลโซโซม ยังส่งผลต่อสรีรวิทยาและการทำงานของไมโตคอนเดรีย ซึ่งนำไปสู่ตัวอย่างเช่น ไมโทฟาจีบกพร่อง ฟอสโฟรีเลชั่นออกซิเดชันที่ผิดปกติ, ไดนามิกของไมโตคอนเดรียที่ควบคุมไม่ได้, ไมโทเจเนซิสที่เปลี่ยนแปลง, ความไม่สมดุลของแคลเซียม, การค้ายลที่เปลี่ยนแปลงไปและการเหนี่ยวนำให้เกิดความเครียดออกซิเดชัน (ตารางที่ 2) เส้นทาง autophagy ที่ไม่ขึ้นกับ PRKN นั้นเกี่ยวข้องกับกระบวนการไมโทฟาจีแบบเลือกผ่านผ่านตัวรับสื่อกลาง ลิพิด และ ubiquitin ligase-mediated pathways [97,139,140] ปัจจุบันยังไม่เป็นที่ทราบแน่ชัดว่าเส้นทางเหล่านี้เชื่อมโยงกับ PD มากน้อยเพียงใด
บทความนี้คัดมาจาก Cells 2021, 10, 3547 https://doi.org/10.3390/cells10123547 https://www.mdpi.com/journal/cells






