การค้นพบและการระบุองค์ประกอบที่มีศักยภาพในการต่อต้านการสร้างเม็ดสีของ Bletilla Striata
Mar 26, 2022
ali.ma@wecistanche.com
Yiyuan Luo1, Juan Wang1, Shuo Li1, Yue Wu1, Zhirui Wang1, Shaojun Chen1 และ Hongjiang Chen1,2*
เชิงนามธรรม
พื้นหลัง:Bletilla striata เป็นยาหลักของสูตรคลาสสิกของผิวขาวจำนวนมากในการแพทย์แผนจีน (TCM) และมีการใช้กันอย่างแพร่หลายในอุตสาหกรรมเครื่องสำอางเมื่อเร็ว ๆ นี้ อย่างไรก็ตาม สารออกฤทธิ์ยังคงไม่ชัดเจนและรากที่มีเส้นใยของมันยังใช้ไม่ได้ผลอย่างมีประสิทธิภาพ จุดมุ่งหมายของการศึกษาครั้งนี้คือการค้นหาและระบุองค์ประกอบที่ออกฤทธิ์ต่อต้านการสร้างเม็ดสีโดยแบบจำลองม้าลายและการเทียบท่าระดับโมเลกุล
วิธีการ:ดิสารต้านอนุมูลอิสระกิจกรรมถูกประเมินโดย 2,2-diphenyl-1-picrylhydrazyl (DPPH) Radical scavengingactivity, 2,2′-azino-bis-(3-ethylbenthiazoline-6-sulphonic acid) (ABTS) ) กิจกรรมการขจัดอนุมูลอิสระและการลดเฟอริกสารต้านอนุมูลอิสระการทดสอบกำลัง (FRAP) ประเมินฤทธิ์ต้านการสร้างเม็ดสีโดยไทโรซิเนสตัวยับยั้งกิจกรรมในหลอดทดลองและยับยั้งเมลานินในปลาม้าลาย โพรไฟล์ทางเคมีถูกดำเนินการโดยโครมาโตกราฟีของเหลวสมรรถนะสูงพิเศษรวมกับแมสสเปกโตรเมทรีตีคู่เวลาบินควอดรูโพล (UPLC-Q-TOF-MS/MS) ในขณะเดียวกัน ส่วนประกอบที่มีศักยภาพในการต่อต้านการสร้างเม็ดสีถูกระบุชั่วคราวโดยการเชื่อมต่อระดับโมเลกุล
ผลลัพธ์:สารสกัดเอธานอล 95 เปอร์เซ็นต์ของราก B. striata fibrous (EFB) มีกิจกรรมการยับยั้ง DPPH, ABTS, FRAP และไทโรซิเนสที่แรงที่สุด โดยมี IC50 5.94 มก./ลิตร, 11.69 มก./ลิตร, 6.92 มิลลิโมล FeSO4/g, และ 58.92 มก./ลิตร ตามลำดับ นอกจากนี้ EFB และสารสกัดเอทานอล 95 เปอร์เซ็นต์ของ B. striata tuber (ETB) ช่วยลดการสังเคราะห์เมลานินของ zebrafishembryos ในลักษณะที่ขึ้นกับขนาดยาอย่างมีนัยสำคัญ องค์ประกอบทางเคมี 39 ชนิด ซึ่งรวมถึงสไตลบีนอยด์ 24 ชนิดถูกระบุอย่างไม่แน่นอนจาก EFB และ ETB การเทียบท่าระดับโมเลกุลบ่งชี้ว่ามีสารประกอบ 83 (รวมถึง 60 สติลบีนอยด์) และ 85 (ซึ่งรวมถึง 70 สติลบีนอยด์) ที่แสดงสัมพรรคภาพการจับที่แรงกว่ากับไทโรซิเนสและอะดีนิเลตไซคเลส
บทสรุป:การค้นพบนี้สนับสนุนเหตุผลในการใช้ EFB และ ETB เป็นสารฟอกสีผิวตามธรรมชาติในอุตสาหกรรมยาและเครื่องสำอาง
คำสำคัญ: Bletilla striata, สารต้านอนุมูลอิสระ, ฤทธิ์ต้านการสร้างเม็ดสี, UPLC-Q-TOF-MS/MS, Zebrafish, การเทียบท่าระดับโมเลกุล

คลิกเพื่อดูผลข้างเคียงและประโยชน์ของสารต้านอนุมูลอิสระ
พื้นหลัง
Bletilla striata (Thunb.) Reichb. ฉ. เป็นไม้ล้มลุกยืนต้นกระจายอยู่ทั่วไปในเอเชีย เช่น จีน เกาหลี และญี่ปุ่น [1] หัวแห้งของ B. striata หรือที่รู้จักในชื่อ Baiji ซึ่งบันทึกครั้งแรกใน Classic of Materia Medica ของ Shennong มีการใช้กันอย่างแพร่หลายในการแพทย์แผนจีน (TCM) เป็นเวลาหลายพันปีในประเทศจีน เภสัชตำรับจีนระบุว่ามีความสามารถในการฝาดในการห้ามเลือดและยาแก้ปวด ดังนั้นจึงใช้กันอย่างแพร่หลายในการรักษาภาวะโลหิตจาง ไอเป็นเลือด เลือดออกจากบาดแผล แผล บวมและผิวหนังแตก [2, 3] การศึกษาทางเภสัชวิทยาแสดงให้เห็นว่า B. striata มีฤทธิ์ทางชีวภาพในวงกว้าง เช่น การรักษาบาดแผล [4, 5], antiulcer [6, 7], ห้ามเลือด [8],ต่อต้าน-การอักเสบ[9], สารต้านอนุมูลอิสระ[10] ต้านแบคทีเรีย [11] ต้านไวรัสไข้หวัดใหญ่ [12] และต่อต้านวัย [13] ในเวลาเดียวกัน B. striata มีองค์ประกอบทางเคมีหลายประเภท ได้แก่พอลิแซ็กคาไรด์[14], ไบเบนซิล, ฟีแนนทรีน, แอนทราควิโนน,ฟลาโวนอยด์และ 2-ไอโซบิวทิลมาเลต [3, 15] เป็นต้น
B. striata เป็นยาหลักของผิวขาวหลายสูตรคลาสสิกใน TCM [16] และมีการใช้กันอย่างแพร่หลายในอุตสาหกรรมเครื่องสำอางเมื่อเร็ว ๆ นี้ [17] อย่างไรก็ตาม ส่วนผสมออกฤทธิ์ของมันยังคงไม่ชัดเจนและแม้แต่ผลการวิจัยบางอย่างก็ขัดแย้งกัน ตัวอย่างเช่น ผลการวิจัยที่ได้รับจาก Chenet al. ระบุว่าสารสกัดเอทานอล 95 เปอร์เซ็นต์ของ B. striata มีฤทธิ์ยับยั้งไทโรซิเนสสูงกว่าสารสกัดน้ำที่มีอัตราการยับยั้ง 68.36 เปอร์เซ็นต์ ในหลอดทดลอง [18] ในขณะที่ผลของ Huang et al. พบว่าฤทธิ์การยับยั้งของสารสกัดจากน้ำ B. striata บนไทโรซิเนสนั้นแรงกว่าสารสกัดเอธานอล 95 เปอร์เซ็นต์ภายในอัตราการยับยั้ง 62 เปอร์เซ็นต์ในหลอดทดลอง [19] ผลการวิจัยโดย Luetal [20]และLinghuetal [21] แสดงให้เห็นว่าทั้งน้ำและสารสกัดเอธานอล 95 เปอร์เซ็นต์ของ B. striata โดยเฉพาะอย่างยิ่งการแยกคลอโรฟอร์มสามารถยับยั้งการเจริญเติบโตของเซลล์ B16 และกระตุ้นการตายของเซลล์ในลักษณะที่ขึ้นกับความเข้มข้น
เนื่องจากการทดสอบในหลอดทดลองของการยับยั้งไทโรซิเนสและสายเซลล์เมลาโนมา ไม่เกี่ยวข้องกับสภาวะทางสรีรวิทยาที่ซับซ้อนในร่างกาย และการดูดซึม เมแทบอลิซึม การกระจายและการขับถ่ายของตัวอย่างทดสอบ ตัวอย่างจำนวนมากแสดงฤทธิ์ยับยั้งที่มีนัยสำคัญต่อไทโรซิเนสและเซลล์เมลาโนมาใน หลอดทดลอง,อย่างไรก็ตาม,จัดแสดงอย่างมีประสิทธิภาพน้อยหรือแม้ไม่ได้ผล ในร่างกาย [22,23]. กลาบริดินแสดงฤทธิ์ยับยั้งไทโรซิเนสอย่างมีนัยสำคัญกับ IC50 0.43μmol/L ซึ่งแรงกว่ากรดโคจิก 176 เท่า อย่างไรก็ตาม มันไม่มีผลยับยั้งการสร้างเม็ดสีของ zebrafish ในร่างกาย[24]
ในขณะเดียวกัน B. striata fibrous root (FB) เป็นผลพลอยได้ที่เกิดขึ้นระหว่างการประมวลผลของ B. striatatuber (TB) การวิจัยสมัยใหม่ระบุว่า FB มีสารประกอบที่คล้ายคลึงกันกับวัณโรคและมีปริมาณฟีนอลสูงกว่า [25] นอกจากนี้ ฤทธิ์ต้านแบคทีเรีย [26] สารต้านอนุมูลอิสระและฤทธิ์ต้านไทโรซิเนสของสารสกัด FB นั้นแข็งแกร่งกว่าสารสกัด TB [25] อย่างไรก็ตาม ทรัพยากรของ FB ไม่ได้ถูกใช้อย่างมีประสิทธิภาพและถูกละทิ้งในพื้นที่การเกษตร ซึ่งทำให้สิ้นเปลืองทรัพยากร FB และมลภาวะต่อสิ่งแวดล้อม [27]
Zebrafish (Danio rerio) ปลาน้ำจืดเขตร้อนขนาดเล็กเป็นสัตว์ต้นแบบสำหรับเภสัชวิทยา
และการวิจัยด้านพิษวิทยาในร่างกาย ซึ่งมีข้อดีหลายประการ ได้แก่ ต้นทุนต่ำ วงจรชีวิตสั้น ความโปร่งใสสูง ดูแลรักษาง่าย ความอุดมสมบูรณ์สูง และต้องการตัวอย่างการทดสอบน้อยลง [28, 29] นอกจากนี้ zebrafish ยังมีเม็ดสีเมลานินอยู่บนพื้นผิว ทำให้สังเกตกระบวนการสร้างเม็ดสีได้ง่าย และถูกนำมาใช้กันอย่างแพร่หลายในการศึกษาต่อต้านการสร้างเม็ดสี [28, 30]
ในการศึกษานี้ เราเปรียบเทียบฤทธิ์ต้านอนุมูลอิสระและฤทธิ์ยับยั้งไทโรซิเนสของสารโพลีแซ็กคาไรด์แบบหยาบกับสารสกัดเอธานอล 95 เปอร์เซ็นต์ของ TB และ FB ในหลอดทดลอง และฤทธิ์ต้านการสร้างเม็ดสีในแบบจำลองปลาม้าลาย ในขณะเดียวกัน องค์ประกอบที่ออกฤทธิ์ต่อต้านเมลาโนเจนที่อาจเกิดขึ้นนั้นถูกระบุชั่วคราวโดยการเทียบท่าระดับโมเลกุล เราค้นพบว่าสารสกัดเอธานอล 95 เปอร์เซ็นต์ของ TB (ETB) และ FB(EFB) มีสารต้านอนุมูลอิสระและฤทธิ์ต้านไทโรซิเนสอย่างมีนัยสำคัญ และสามารถลดการสังเคราะห์เมลานินของตัวอ่อนของ zebrafish ในลักษณะที่ขึ้นกับขนาดยา ดังนั้น ETB และ EFB จึงสามารถใช้เป็นสารฟอกสีผิวตามธรรมชาติในอุตสาหกรรมยาและเครื่องสำอาง
วิธีการ
เคมีภัณฑ์และรีเอเจนต์
ไทโรซิเนส 3-(3,4-dihydroxyphenyl)-L-alanine(L-DOPA) และ arbutin ถูกซื้อจากบริษัทตัวทำปฏิกิริยาอะลาดิน (เซี่ยงไฮ้ ประเทศจีน)2,2-ไดฟีนิล{{8 }}พิคริลไฮดราซิล (DPPH), 2,2′-azino-bis-(3-เอทิลเบนไทโซลีน-6-กรดซัลโฟนิก) (ABTS),6-ไฮดรอกซี-2,5,7 ,8-tetramethylchroman-2-carboxylic acid(Trolox) และ 2,4,6-tris (2-pyridyl)-s-triazine (TPTZ) ถูกซื้อจาก Sigma-Aldrich (เซนต์หลุยส์ มิสซูรี สหรัฐอเมริกา). ซื้ออะซิโตไนไตรล์และเมทานอล (เกรด HPLC) จาก Tedia (แฟร์ฟิลด์ รัฐโอไฮโอ สหรัฐอเมริกา) น้ำปราศจากไอออนถูกเตรียมโดยระบบน้ำ Milli-Q (18.2 MΩ, Millipore, USA)
ขั้นตอนการรวบรวมและสกัดพืช
B. striata รวบรวมจาก Quzhou YiNianTang Agriculture and Forestry Technology Co., Ltd. (Quzhou เจ้อเจียง จีน) ตัวอย่างบัตรกำนัลถูกเก็บไว้ที่สมุนไพรของวิทยาลัยเภสัชกรรมเจ้อเจียง (ภาคยานุวัติเลขที่ 190615) พืชทั้งหมดถูกแบ่งออกเป็นหัวและรากที่มีเส้นใย ต่อจากนั้นก็หั่นเป็นชิ้นเล็กๆ และทำแห้งโดยการทำแห้งเยือกแข็งแบบสุญญากาศตามลำดับ
ตัวอย่างที่แห้งและเป็นผง (TB และ FB) ถูกสกัดด้วยกรดไหลย้อนด้วยเอทานอล 95 เปอร์เซ็นต์ สามครั้ง (1.5 ชั่วโมงต่อครั้ง) สารสกัดถูกกรองโดยใช้กระดาษกรอง What man (ฉบับที่ 1) สิ่งกรองถูกทำให้แห้งแบบเข้มข้นในเครื่องระเหยแบบหมุน (Hei-VAP, ไฮดอล์ฟ, เยอรมนี) ที่ 50 องศาและถูกทำให้แห้งในเวลาต่อมาโดยเครื่องทำแห้งแบบสุญญากาศ ผลผลิตเอทานอลสกัดของ TB (ETB) และ FB (EFB) เท่ากับ 5.21 และ 6.53 เปอร์เซ็นต์ ตามลำดับ กากตะกอนถูกใช้เพื่อสกัดพอลิแซ็กคาไรด์ดิบโดยแยกย้ายกันไปในน้ำ 80 องศาเป็นเวลา 4 ชั่วโมงและตกตะกอนด้วยเอทานอล [31] ผลผลิตพอลิแซ็กคาไรด์ของ TB (PTB) และFB (PFB) เท่ากับ 14.75 และ 6.45 เปอร์เซ็นต์ ตามลำดับ

สารสกัดจากซิสแทนเช่
การวิเคราะห์ทางเคมี
การวิเคราะห์ทางเคมีถูกดำเนินการบนโครมาโตกราฟีของเหลวสมรรถนะสูงพิเศษที่รวมกับแมสสเปกโตรเมทรีตีคู่เวลาบินควอดรูโพล (UPLC-Q-TOF-MS/MS) การแยกโครมาโตกราฟีดำเนินการบน Waters Acquity UPLC tem (Waters Corp., Milford, MA, US) ด้วยคอลัมน์ WatersBEH Shield RP C18 (100×2.1mm, 1.7μm) ที่3{ {43}} องศา เฟสเคลื่อนที่ประกอบด้วยฟอร์มิคาซิด 0.1 เปอร์เซ็นต์ในน้ำ (A) และอะซิโตไนไทรล์ (B) โดยมีเกรเดียนต์เชิงเส้น: 0–3 นาที, 5–16 เปอร์เซ็นต์ B; 3–8 นาที, 16–30 เปอร์เซ็นต์ ข; 8–10 นาที 30–35 เปอร์เซ็นต์ ข; 10–15 นาที 35–55 เปอร์เซ็นต์ ข; 15–18 นาที, 55–80 เปอร์เซ็นต์ ข; 18–19 นาที, 80–5 เปอร์เซ็นต์ ข; 19–20 นาที, 5 เปอร์เซ็นต์ B. อัตราการไหลคือ 0.3 มล./นาที และปริมาตรการฉีดคือ 2 ไมโครลิตร
การทดลอง TOF-MS/MS ถูกดำเนินการโดยใช้แมสสเปกโตรเมทรี AB SCEIX Triple TOF 5600 (AB SCIEX, ฟอสเตอร์ซิตี, แคลิฟอร์เนีย, สหรัฐอเมริกา) ที่ติดตั้งแอนอิเล็กโทรสเปรย์ไอออไนซ์ (ESI) การตรวจจับ MS ดำเนินการด้วยวิธีไอออนไนซ์เชิงลบ พารามิเตอร์ถูกกำหนดดังนี้: อุณหภูมิแหล่งที่มาและการสลายตัวคือ 100 องศาและ 450 องศาตามลำดับ; อัตราการไหลของก๊าซที่ละลายในน้ำคือ 900L/h; แรงดันเส้นเลือดฝอยคือ 2kV; แรงดันกรวยคือ 40 V; พลังงานปะทะ 22 eV; และ scanspectra แบบเต็มคือตั้งแต่ 100 ถึง 2000 Da
สารต้านอนุมูลอิสระตรวจสอบกิจกรรมการขจัดอนุมูลอิสระ DPPH
กิจกรรมการกำจัดอนุมูลอิสระของ DPPH ถูกกำหนดให้ไม่สอดคล้องกับ Ali et al โดยมีการปรับเปลี่ยนเล็กน้อย [32] โดยสรุป สารละลายตัวอย่างทดสอบ 50 μL ถูกผสมกับสารละลายเอทานอล 150 μLDPPH (0.2mM) ในเพลต 96-หลุม และถูกเก็บไว้ในที่มืดเป็นเวลา 30 นาที . การดูดกลืนแสงของส่วนผสมที่ 517 นาโนเมตร (A1) ได้รับการประเมินโดยไมโครเพลทสเปกโตรโฟโตมิเตอร์ (Thermo Fisher Scientific, America) สารละลายเปล่าที่ไม่มีตัวอย่างทดสอบที่ผสมกับสารละลาย DPPHethanol ถูกกำหนดให้เป็นกลุ่มบวก (A0) สารละลายเปล่าที่ไม่มี DPPH ผสมกับสารละลายตัวอย่างทดสอบถูกตั้งค่าเป็นกลุ่มว่าง (A2) การทดลองทั้งหมดดำเนินการเป็นสามเท่า อัตราการกำจัดอนุมูลอิสระ DPPH คำนวณโดยใช้สูตรต่อไปนี้:
อัตราการกำจัดอนุมูล DPPH ( เปอร์เซ็นต์ ) {{0}} [A0-(A1-A2)]/A0 × 100 เปอร์เซ็นต์
กิจกรรมกำจัดอนุมูลอิสระของ ABTS
วัดความสามารถในการกำจัดอนุมูลอิสระของ ABTS โดยใช้วิธีการที่อธิบายโดย Ali et al [32]. โดยย่อ สารละลายในน้ำ 7mMABST ถูกผสมกับโพแทสเซียม เพอร์ซัลเฟต 2.45 มิลลิโมลาร์ที่อัตราส่วน 1:1 (ปริมาตร/ปริมาตร) และบ่มที่อุณหภูมิห้องในที่มืดเป็นเวลา 16 ชั่วโมงเพื่อให้ได้สารละลาย ABST บวกกับสต็อก สารละลายสต็อกถูกเจือจางด้วยน้ำเกลือที่บัฟเฟอร์ด้วยฟอสเฟต (PBS) เพื่อปรับการดูดกลืนแสงของ(0.72±0.2) ที่ 734 นาโนเมตร ตัวอย่างทดสอบ 20μL ที่ความเข้มข้นต่างกันถูกผสมอย่างละเอียดด้วยสารละลาย 180μL ABTS plus ของผสมปฏิกิริยาถูกเก็บไว้ในที่มืดเป็นเวลา 5 นาที และต่อมาวัดค่าการดูดกลืนแสง (B1) ที่ 734 นาโนเมตร การดูดกลืนแสงของของผสมที่ไม่มีตัวอย่างทดสอบและ ABST plus ถูกกำหนดเป็น B และ B ตามลำดับ การทดลองทั้งหมดดำเนินการเป็นสามเท่า อัตราการขจัดอนุมูล ABTS คำนวณตามสูตรต่อไปนี้:
อัตราการขจัดอนุมูล ABTS ( เปอร์เซ็นต์ ) {{0}} [B0-(B1-B2)]/B0 × 100 เปอร์เซ็นต์
การทดสอบฤทธิ์ต้านอนุมูลอิสระของเฟอริกรีดิวซ์ (FRAP)
กิจกรรมการลดธาตุเหล็กเฟอริกถูกกำหนดตามขั้นตอนโดย Kosakowska และคณะ [33]. 300mM อะซิเตทบัฟเฟอร์, 10mM TPTZ (2,4,6-ทริส (2-ไพริดิล)-s-ไตรอะซีน)และ 20mM FeCl3 ถูกผสมที่ (v/v/v) อัตราส่วน 10:1:1 เพื่อเตรียมสารทำงาน 100μL ของสารละลายตัวอย่างทดสอบแต่ละอย่างผสมกับน้ำยาทำงาน 100μL TPTZ บ่มที่ 37 องศาเป็นเวลา 20 นาทีและกำหนดค่าการดูดกลืนแสงที่ 593 นาโนเมตร ในขณะเดียวกัน ชุดของสารละลายมาตรฐาน FeSO4 ในช่วงความเข้มข้น 0–1000ug/mL ถูกใช้เพื่อเตรียมกราฟการปรับเทียบ ความสามารถในการรีดิวซ์ของเฟอริกคำนวณในรูปแบบของสารเชิงซ้อนสีน้ำเงิน Fe2 บวก -TPTZ เข้มข้น ผลลัพธ์ถูกแสดงเป็น Fe2 บวกความสามารถในการต้านอนุมูลอิสระ (มิลลิโมล FeSO4/g ของสารสกัด)
ฤทธิ์ยับยั้งไทโรซิเนส
กิจกรรมการยับยั้งไทโรซิเนสถูกกำหนดโดยวิธีสเปกโตรโฟโตเมตริกโดยใช้ L-DOPA เป็นสารตั้งต้น [34] โดยสรุป สารละลายตัวอย่าง50μLที่ความเข้มข้นต่างกันผสมกับไทโรซิเนส 50 ไมโครลิตร (200 หน่วย/มิลลิลิตร, pH ที่ละลายในบัฟเฟอร์ 6.8 ฟอสเฟต) ใน 96-หลุม แผ่นและฟักเป็นเวลา 15 นาทีที่ 25 องศา จากนั้นปฏิกิริยาเริ่มต้นด้วยการเติม L-DOPA (50 ไมโครลิตร) หลังจากการฟักตัว 30 นาทีที่ 25 องศา การดูดกลืนแสงที่ 490 นาโนเมตร (Aa) ถูกกำหนดโดยใช้ไมโครเพลทสเปกโตรโฟโตมิเตอร์ท้องฟ้าแบบมัลติสแคน (ThermoFisher Scientific, America) ในทำนองเดียวกัน การดูดกลืนแสงของหลุมตัวอย่างที่ไม่มีไทโรซิเนส (Ab) และหลุมควบคุมที่มีเอนไซม์แต่ไม่มีตัวอย่าง (Ab) ถูกตรวจพบในเวลาเดียวกัน กิจกรรมการยับยั้งไทโรซิเนสคำนวณโดยสมการดังต่อไปนี้:
อัตราการยับยั้งไทโรซิเนส ( เปอร์เซ็นต์ )=[1− (Aa − Ab)/Ac] × 100 เปอร์เซ็นต์
IC50 คำนวณโดยใช้สมการ GraphPad Prism ดังนี้:
Y=นาทีบวก (สูงสุด − นาที)/1 บวก 10(x−logIC50)×เนินลาด
X แสดงถึงความเข้มข้นของตัวยับยั้ง Y แสดงข้อมูลการยับยั้ง ( เปอร์เซ็นต์ ) พร้อมกับค่าต่ำสุด (ต่ำสุด) และสูงสุด (สูงสุด) ความลาดชันของเนินเขาคือความชัน

Cistanche ยับยั้งการทำงานของไทโรซิเนส
การยับยั้งเมลานินในปลาม้าลาย
ปลาม้าลาย AB สายพันธุ์ป่า (จัดหาโดย Hunter Bio-technology, Inc., หางโจว, จังหวัดเจ้อเจียง) เลี้ยงในน้ำปลา (0.2 เปอร์เซ็นต์เกลือสมุทรสำเร็จรูปในน้ำปราศจากไอออน, pH 6.9–7.2, การนำไฟฟ้า 48{ {18}}–510 mS/ซม. และความแข็ง 53.7–71.6 มก./ลิตร CaCO3) ในช่วงแสง/มืด 14/10 ชม. ที่อุณหภูมิคงที่ 28±0.5 องศา และให้อาหารกุ้งน้ำเกลือที่มีชีวิตวันละสองครั้ง ได้มาจากการวางไข่ตามธรรมชาติและรวบรวมไว้ภายใน 30 นาที การทดสอบ zebrafish ได้รับการรับรองโดย Association for Assessment and Accreditation of Laboratory Animal Care (AAALAC) การศึกษาปัจจุบันได้รับการอนุมัติโดย IACUC (Institutional Animal Careand Use Committee) ที่ Hunter Biotechnology, Inc. และหมายเลขการอนุมัติ IACUC คือ 001458
ตัวอ่อนที่ระยะ 6 ชั่วโมงหลังการปฏิสนธิ (hpf) ได้รับการรักษาสารสกัดแต่ละสารสกัดที่ความเข้มข้นหกระดับ (10, 30, 62.5,125, 250 และ 500 มก./ลิตร) เป็นเวลา 72 ชั่วโมงเพื่อประเมินความเข้มข้นที่ไม่เป็นอันตรายสูงสุด (MNLC) ). ผลที่ได้คือ MNLC ของสารสกัดทั้งหมดมีเอ็มบริโอมากกว่า 62.50 มก./ลิตร 10 ตัวถูกวางไว้ใน 6-หลุม และสัมผัสตัวอย่างที่ทดสอบแล้วที่ความเข้มข้น 10 และ 30 มก./ลิตร ตั้งแต่ 6 แรงม้า ถึง 54 แรงม้า (การได้รับสัมผัส 48 ชั่วโมง) ). DMSO (0.05 เปอร์เซ็นต์ ปริมาตร/ปริมาตร) แอนดาบูติน (10 และ 30 มก./ลิตร) ถูกใช้เป็นกลุ่มควบคุมปกติและเชิงบวก ตามลำดับ
รวบรวมและสังเกตเอ็มบริโอที่ซิงโครไนซ์ภายใต้กล้องสเตอริโอไมโครสโคป (SZX7, Olympus, Japan) ที่ติดตั้งกล้องดิจิตอล (VertA1, China) การสะสมของเมลานินซึ่งมีความสัมพันธ์โดยตรงกับบริเวณที่เกิด zebrafishpigmentation คำนวณโดยใช้ GNUImage Manipulation Program (GIMP เวอร์ชัน 2.10.2) และแสดงเป็นเปอร์เซ็นต์เทียบกับกลุ่มควบคุมเชิงลบ (การสะสมเมลานิน 100 เปอร์เซ็นต์ ) [28, 30]
การศึกษาเทียบท่าระดับโมเลกุล
158 สารประกอบที่แยกได้จาก B. striata ในวรรณคดี[2] รวมถึง 19 ไกลโคไซด์ 28 ไบเบนซิลส์ 19 ฟีแนน-ทรีนส์ 18 ไบฟีแนนทรีน 23 ไดไฮโดรฟีแนนทรีน 5 แอนโธไซยานิน 11 สเตียรอยด์ 8 ไตรเทอร์พีนอยด์ กรดฟี-นอลิก 12 ตัว 5 ควิโนน และสารประกอบอื่นอีก 10 ชนิด ถูกใช้เป็นลิแกนด์ โครงสร้าง 3 มิติถูกวาดโดย ChemBio3D และได้รับการปรับให้เหมาะสมโดยใช้ MM2 และเครื่องมือ Autodock โครงสร้างผลึกสามมิติของไทโรซิเนส (PDBID:5M8N) และอะดีนิเลตไซโคลส (PDB ID:5IV3) ถูกดึงมาจาก RCSB Protein Data Bank (www.rcsb.org/pdb/home/home.do) โมเลกุลของน้ำและอะตอมต่างชนิดกันทั้งหมดถูกกำจัดออกจากโครงสร้างผลึกโดยใช้เครื่องมือ Chimera และ MGL ในที่สุด Autodock
Vina ถูกใช้เพื่อเทียบเคียงโปรตีนตัวรับกับลิแกนด์โมเลกุลขนาดเล็ก พารามิเตอร์ของตำแหน่งเชื่อมต่อโปรเทอินรีเซพเตอร์ถูกกำหนดเป็น −36.700, 7.034, −19.104 และ − 17.467, − 22.807, 2.786 ตามลำดับ ตามลิแกนด์ไมโมซีนดั้งเดิมและ LRE1 [35] เพื่อให้ได้ความแม่นยำในการคำนวณที่สูงขึ้น พารามิเตอร์ความละเอียดถี่ถ้วน 20 พารามิเตอร์สำหรับตัวรับแต่ละตัวจึงถูกสร้างขึ้น และโครงสร้างที่มีความสัมพันธ์กันสูงสุดถูกเลือกเป็นโครงสร้างการเทียบท่าขั้นสุดท้ายและแสดงให้เห็นใน Pymol2.3 ในขณะเดียวกัน mimosine ลิแกนด์ดั้งเดิมและ LRE1 ถูกนำมาใช้เป็นตัวควบคุมเชิงบวก [36]
ในการทำนาย ADMET ของ silico
การตี 3 อันดับแรกจาก B. striata มีสัมพรรคภาพการจับที่ดีกว่ากับไทโรซิเนสและอะดีนิเลตไซคเลส อยู่ภายใต้การวิเคราะห์ ADMET QikProp ใน Schrodingersuite ใช้ในการคำนวณคุณสมบัติทางกายภาพและลักษณะที่เกี่ยวข้องกับยา ซึ่งรวมถึงน้ำหนักโมเลกุล (MW) ค่าสัมประสิทธิ์การแบ่งส่วนออกทานอล/น้ำ (QPlogPo/w) ที่คาดการณ์ไว้ ความสามารถในการละลายในน้ำที่คาดการณ์ไว้ (QPlogS) เซลล์ Caco-2 ที่คาดการณ์ไว้ การซึมผ่านของผนังกั้นลำไส้ (QPPCaco) ค่าสัมประสิทธิ์การแบ่งตัวของสมอง/เลือดที่คาดการณ์ (QPlogBB) ความสามารถในการซึมผ่านของผิวหนังที่คาดการณ์ไว้ (QPlogKp) การคาดการณ์ IC50 สำหรับการอุดตันของช่อง HERGK บวก (QPlog HERG) และการคาดการณ์การดูดซึมราในมนุษย์ คุณสมบัติได้รับการประเมินตามกฎของ Lipin-ski ห้าข้อและวรรณกรรม [37, 38]
การจำลองพลวัตของโมเลกุล
เพื่อตรวจสอบความเสถียรและความผันผวนแบบไดนามิกของสารเชิงซ้อนลิแกนด์-โปรตีนภายใต้สภาพแวดล้อมทางชีวภาพจำลอง และตรวจสอบผลการเทียบท่าเพิ่มเติม สารประกอบ blestrin D (75) ได้รับเลือกให้เป็นลิแกนด์สำหรับการศึกษาแบบจำลองพลวัตของโมเลกุล (MD) โดยอิงจาก ผลการเทียบท่าของโมเลกุล คอมเพล็กซ์ของ blestrin D ที่มี tyrosinase และ adenylate cyclase ได้ดำเนินการจำลอง MD และรันเป็นเวลา 100ns โดยใช้โหมดน้ำ TIP3P ค่าเบี่ยงเบนกำลังสองเฉลี่ยของราก (RMSD) ของอะตอมของกระดูกสันหลังของโปรตีนที่สัมพันธ์กับโครงสร้างเริ่มต้นถูกคำนวณเพื่อตรวจสอบความคงตัวของโปรตีนตลอดระยะเวลาการจำลอง [39]
ผลลัพธ์
องค์ประกอบทางเคมี
โครมาโตแกรมโครมาโตแกรมพื้นฐานทั่วไปของ ETB และ EFB แสดงในรูปที่ 1 ซอฟต์แวร์ PeakView ใช้เพื่อระบุองค์ประกอบ สูตรโมเลกุลถูกกำหนดอย่างแม่นยำภายในข้อผิดพลาดของมวล 10ppm น้ำหนักโมเลกุลที่แน่นอนและการแยกส่วนถูกใช้เพื่อระบุส่วนประกอบตามวรรณกรรมและฐานข้อมูลโครงสร้างทางเคมีอิสระ เช่น ChemSpider และ Massbank ผลที่ได้คือ องค์ประกอบทางเคมี 39 ชนิด ซึ่งรวมถึงสไตลบีนอยด์ 24 ชนิด (ไบเบนซิล ฟีแนนทรีนและอนุพันธ์ของพวกมัน) 6 ไกลโคไซด์ กรด 4ฟีนอล 3 ควิโนน สเตียรอยด์ 1 ตัว และสารประกอบอื่นอีก 1 ชนิดถูกระบุอย่างไม่แน่นอนจาก EFB และ ETB ในเวลาเดียวกัน การหาปริมาณกึ่งเชิงสัมพัทธ์ของพวกมันถูกดำเนินการโดยการวัดพื้นที่พีคของสารประกอบแต่ละโหมดในโหมด MS โดยใช้โครมาโตแกรมของไอออนที่แยกออกมา [40] ข้อมูลโดยละเอียดของการระบุและเนื้อหาที่เกี่ยวข้อง (ไฮไลท์แผนที่ความร้อน ยิ่งสีเข้มขึ้นเท่าใด ความเข้มข้น) สรุปไว้ในตารางที่ 1

มะเดื่อ 1โครมาโตแกรมเบสพีคของเอทานอลร้อยละ 95 สกัดจากB. striataหัว (A) และรากที่มีเส้นใย (B)
ความสามารถในการต้านอนุมูลอิสระ
เป็นที่ทราบกันดีว่าการฉายรังสีอัลตราไวโอเลต A (UVA) สามารถกระตุ้นการผลิตออกซิเจนชนิดปฏิกิริยา (ROS) และไกล่เกลี่ยการสร้างเม็ดสีที่มากเกินไปในเซลล์ผิวหนัง โพลีฟีนอลธรรมชาติเป็นตัวยับยั้งการสร้าง ROS และอาจมีหน้าที่ในการต่อต้านการสร้างเม็ดสีของสารสกัดจากพืช [41 , 42. ดังนั้นในการศึกษานี้ ความสามารถในการต้านอนุมูลอิสระจึงถูกประเมินผ่าน DPPH กิจกรรมการขับอนุมูลอิสระของ ABTS และ FRAPassay ผลลัพธ์ (ตารางที่ 2 และรูปที่ 2) แสดงให้เห็นว่า EFB (IC50=5.94 มก./ลิตร) มีกิจกรรมการกำจัด DPPHradical ที่แข็งแกร่งที่สุดในหลอดทดลองเมื่อเปรียบเทียบกับ PTB(IC50=548.24 มก./ลิตร) , PFB (IC50=285.81 มก./ลิตร) และ ETB(IC50=65.25 มก./ลิตร) พบแนวโน้มที่คล้ายกันในการทดสอบ ABTS และ FRAP สารสกัดเอธานอลร้อยละ 95 ของ TB และ PB มีฤทธิ์ต้านอนุมูลอิสระในหลอดทดลองที่แข็งแกร่งกว่าโพลีแซ็กคาไรด์แบบหยาบ นอกจากนี้ EFB ยังแสดงฤทธิ์ต้านอนุมูลอิสระที่แข็งแกร่งกว่า ETB ซึ่งสอดคล้องกับผลการวิจัยก่อนหน้านี้ [25]
ฤทธิ์ยับยั้งไทโรซิเนส
ไทโรซิเนสเป็นเอ็นไซม์จำกัดอัตราที่สำคัญในวิถีการสังเคราะห์เมลานินและถูกใช้อย่างกว้างขวางเพื่อระบุศักยภาพของผลิตภัณฑ์จากธรรมชาติที่มีฤทธิ์ต้านการสร้างเม็ดสี [43] ผลลัพธ์ (รูปที่ 3) แสดงให้เห็นว่า ETB และEPB มีฤทธิ์ยับยั้งไทโรซิเนสที่แรงกว่า PTBand PPB ในหลอดทดลอง ซึ่งสอดคล้องกับผลการวิจัยก่อนหน้านี้ [25] EFB แสดงฤทธิ์การยับยั้งไทโรซิเนสที่แรงขึ้นในลักษณะที่ขึ้นกับขนาดยา (ระหว่าง 20 ถึง 200 มก./ลิตร) ที่มี IC50=58.92 มก./ลิตร มากกว่า ETB(IC50=75.44 มก./ลิตร) และอาร์บูตินที่เป็นสารประกอบที่เป็นบวก (IC{ {11}}.02 มก./ลิตร).
การยับยั้งเมลานินในปลาม้าลาย
Zebrafish are recognized as a highly advantageous vertebrate model system to evaluate anti-melanogenesis activity, as it possesses similar organ systems and gene sequences to human beings [28]. Therefore, zebrafish was used to evaluate the anti-melanogenesis activity. As shown in Fig. 4, a large number of melanin (black spots) deposited in the zebrafish embryo in the control and 0.05% DMSO group. The microscopy images showed there was no significant difference in total melanin content between two groups (p>{{0}}.05) ซึ่งบ่งชี้ว่า DMSO 0.05 เปอร์เซ็นต์ของพาหนะนั้นไม่ส่งผลต่อการผลิตเมลานินในตัวอ่อนของปลาม้าลาย อย่างไรก็ตาม หลังจากการสัมผัสกับตัวอย่างที่ทดสอบและอาร์บูตินเป็นเวลา 48 ชั่วโมง ตัวอ่อนของม้าลายจะยับยั้งการสะสมของเมลานินในระดับต่างๆ (รูปที่ 3B,4) ยกเว้นกลุ่ม PFB 10 มก./ลิตร เป็นที่สังเกตได้ว่าปริมาณเมลานินที่เกี่ยวข้องในกลุ่ม ETB 10 มก./ลิตร (78.38 เปอร์เซ็นต์ ) และ 30 มก./ลิตร (64.72 เปอร์เซ็นต์) มีค่าต่ำกว่าในกลุ่ม PTB 10 มก./ลิตร (93.06 เปอร์เซ็นต์ ) และ 30 มก./ลิตร (82.02 เปอร์เซ็นต์) อย่างมีนัยสำคัญ (p<0.01). it="" demonstrated="" that="" the="" anti-melanogenesis="" activity="" of="" etb="" was="" superior="" to="" that="" of="" ptb,="" which="" was="" consistent="" with="" the="" tyrosinase="" inhibitory="" activity.="" whereafter,="" it="" is="" noteworthy="" that="" the="" anti-melanogenesis="" activities="" of="" etb="" (81.65,="" 75.61%)="" and="" efb="" (78.38,="" 64.72%)="" were="" stronger="" than="" that="" of="" arbutin="" (93.57,="" 81.48%)="" at="" the="" same="" dose="" of="" 10="" mg/l="" and="" 30="" mg/l="" (p="" <="" 0.01="" or="">
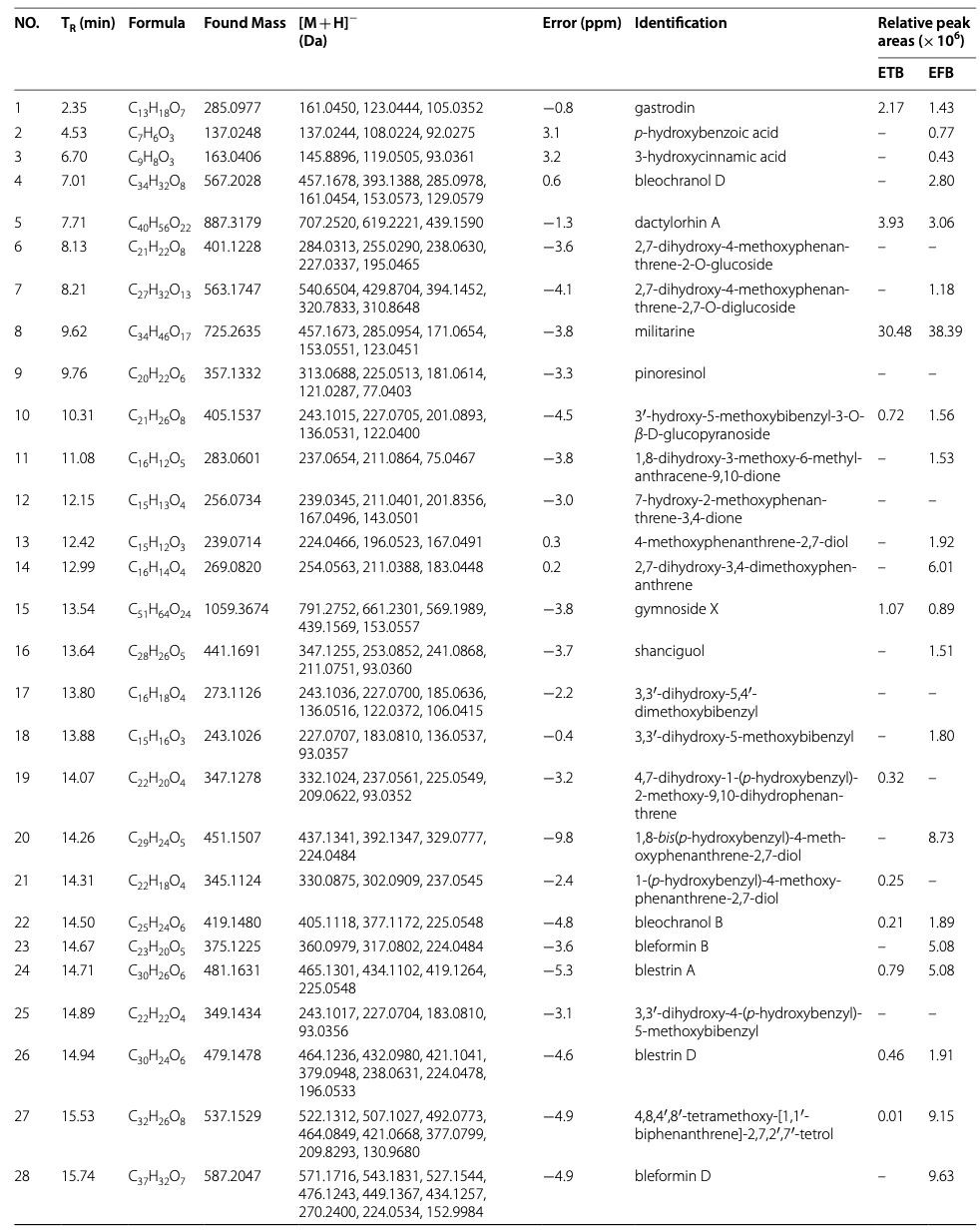
ตารางที่ 1สารประกอบที่ระบุได้จากสารสกัดเอทานอล 95 เปอร์เซ็นต์จากB. striataหัวและรากที่มีเส้นใยโดย UPLC-Q-TOF-MS/MS และพื้นที่พีคสัมพัทธ์
การเทียบท่าระดับโมเลกุล
ไทโรซิเนสเป็นเอนไซม์จำกัดอัตราในการสังเคราะห์เมลานิน: ไฮดรอกซิเลชันของไทโรซีนถึง 3,4-ไดไฮดรอกซี-ฟีนิลอะลานีน (DOPA) และการออกซิเดชันของโดปาควิโนนของ DOPA ดังนั้น ไทโรซิเนสจึงได้รับการพิจารณาว่าเป็นเป้าหมายที่สำคัญสำหรับการพัฒนาสารยับยั้งการสร้างเม็ดสี [44] นอกจากนี้ อะดีนิเลตไซคเลสยังเป็นเอ็นไซม์หลักของการสร้างเมลาโนเจเนซิสที่เกิดจาก cAMP การจับกันของ melanotropin alpha polypeptide (-MSH) กับตัวรับ MC1R ทำให้เกิดการกระตุ้นการทำงานของadenylate cyclase การเพิ่มขึ้นของระดับค่าย การแสดงออกของยีน tyrosinase ที่มีการควบคุมเพิ่มขึ้น และเพิ่มการสังเคราะห์เมลานินในภายหลัง [45] ดังนั้นเราจึงทำการศึกษาการเทียบท่าระดับโมเลกุลของสารประกอบ 158 ตัวที่แยกได้จาก B. striata ก่อนหน้านี้ [2] กับไทโรซิเนสและอะดีนิเลตไซคเลส พลังงานยึดเหนี่ยวของลิแกนด์ที่ศึกษาที่มีไทโรซิเนสและอะดีนิเลตไซคเลสถูกสรุปไว้ในตารางที่ S1 มี 83 (รวมถึง 60 stilbenoids) และ 85 (รวมถึง 70 stilbenoids) ที่มีความสัมพันธ์ในการจับกับไทโรซิเนสและอะดีนิเลตไซคเลสที่แรงกว่าเมื่อเปรียบเทียบกับลิแกนด์ไมโมซีนดั้งเดิม (− 6.4 kcal/mol) และ LRE1 (− 8.5 kcal /โมล). 1,8-บิส(p-ไฮดรอกซีเบนซิล)-4-เมทอกซีฟีแนนทรี-2,7-ไดออล (56), เบลสทริน D (75)และ 2,7-ไดไฮดรอกซี -1,6-bis(p-hydroxybenzyl)-4-meth-oxy-9,10-dihydrophenanthrene (93) เป็นไตรลิแกนด์อันดับต้น ๆ ที่มีต่อไทโรซิเนสโดยมีพลังงานจับ −10.2,10.0 และ 9.7kcal/โมล ตามลำดับ ในขณะที่ blestrin D(75), blestrin B (73) และ 3,3′-dihydroxy-5-methoxy-2,5′,6-tris(p-hydroxybenzyl) bibenzyl (42) เป็นลิแกนด์สามอันดับแรกที่มุ่งสู่อะดีนิเลตไซคเลส โดยมีพลังงานยึดเหนี่ยว − 12.1, − 11.9 และ − 11.6 กิโลแคลอรี/โมล ตามลำดับ สัมพรรคภาพในการจับตามทฤษฎีของพวกมันและอันตรกิริยาของลิแกนด์-อะมิโนแอซิดถูกสรุปไว้ในตารางที่ 3

มะเดื่อ 2DPPH (A) และ ABTS (B) กิจกรรมการกวาดล้างที่รุนแรงของ PTB, PFB, ETB, EFB และ Trolox
เป็นที่น่าสังเกตว่า blestrin D (75) ซึ่งเป็นสารประกอบ biphenanthrene เข้าไปในกระเป๋าจับของtyrosinase และ adenylate cyclase (รูปที่ 5) และแสดงความสัมพันธ์ที่มีนัยสำคัญต่อทั้ง tyrosinase andadenylate cyclase อันตรกิริยาของ Van der Walls ก่อให้เกิดค่าอันตรกิริยาของพลังงานโดยรวม ขณะที่หมู่ไฮดรอกซิลสร้างพันธะไฮโดรเจนกับเรซิดิวกรดอะมิโน Glu 451, Arg114 ของไทโรซิเนส และวาล 167 ของอะดีนิเลตไซโคลสตามลำดับ (ตารางที่ 3 และรูปที่ S1) สารประกอบ 93 ยังแสดงสัมพรรคภาพการจับที่มีนัยสำคัญอีกด้วย ไปสู่ไทโรซิเนสผ่านการก่อรูปของไฮโดรเจนบอนด์ 6 ตัวที่มีเรซิดิวกรดอะมิโน Glu232, Glu451, Ser106,Cys113, Lys223 และ Gln236

มะเดื่อ 3ผลกระทบของสารยับยั้งการสร้างเม็ดสีต่อการทำงานของไทโรซิเนสสัมพัทธ์ (A) การสังเคราะห์ในหลอดทดลองและเมลานิน (B) ในตัวอ่อนของปลาม้าลาย
ในการทำนาย ADMET ของ silico
ค่าที่คาดการณ์ไว้ของพารามิเตอร์ที่สำคัญหลายอย่างพร้อมกับช่วงที่ยอมรับได้นั้นสรุปไว้ในตารางที่ 4 นอกเหนือจาก QPlogS ที่ 3,3′,5-trimethoxybibenzyl, blestrin B และ blestrin D และ QPlogBBof 3,3′,{{6} }trimethoxybibenzyl คุณสมบัติ ADMET ที่คำนวณได้อื่นๆ ทั้งหมดของ Hit สามอันดับแรกนั้นอยู่ในช่วงที่คาดไว้ ในขณะเดียวกัน QPlog HERG ของ Hit สามอันดับแรกทั้งหมดมีค่าน้อยกว่า -5 ซึ่งบ่งชี้ว่าพวกมันมีศักยภาพในการใช้ยาของมนุษย์ QPlog Kp ของความนิยมสูงสุด 3 อันดับแรกสำหรับทั้ง tyrosinase และ adenylatecyclase ยกเว้น 3,3′,5-trimethoxybibenzyl อยู่ในช่วงที่เหมาะสม ซึ่งบ่งชี้ว่าสารประกอบเหล่านี้สามารถเจาะเข้าสู่ผิวหนังได้ง่าย

ตารางที่ 2ผลการวิเคราะห์ฤทธิ์ต้านอนุมูลอิสระในหลอดทดลอง
การจำลองแบบไดนามิกระดับโมเลกุล
พล็อต RMSD แสดงให้เห็นว่าค่า RMSD ของสารเชิงซ้อนโปรตีน-ลิแกนด์ไม่ผันผวนอย่างมีนัยสำคัญตลอดช่วงการจำลองทั้งหมด ค่า RMSD (รูปที่ 6A) ของ blestrin D ที่มีไทโรซิเนสและสารเชิงซ้อนของเอด-ไนเลตไซคเลสถูกกำหนดหาซึ่งมีช่วงตั้งแต่1.5 ถึง 2.8Å และตั้งแต่ 2.0 ถึง 3.6 Å ตามลำดับ ค่า TheRMSF สะท้อนถึงความยืดหยุ่นของแต่ละสิ่งตกค้างระหว่างการจำลอง เรซิดิวที่มีค่า RMSF สูงกว่าเปิดเผยว่าพวกมันมีความยืดหยุ่นมากกว่า (รูปที่ 6B) ค่า RMSF ของเรซิดิวกรดอะมิโนในบริเวณลูปถูกพบว่ามีความผันผวนสูง ในขณะที่สารตกค้างในไซต์ที่ทำงานอยู่ยังคงรักษาค่า RMSF ไว้เล็กน้อย (น้อยกว่า 10Å) เช่น Arg114, Val167, Tyr226, Leu229 และ Arg230in tyrosinase และ Val167, Leu102, Phe45, Lys95 และLeu166 ในอะดีนิเลตไซโคลส บ่งชี้ว่าการผูกกระเป๋าถูกเก็บไว้อย่างมั่นคง ปฏิกิริยาระหว่างโมเลกุลของblestrin D กับ tyrosinase และ adenylate cyclase ถูกแสดงไว้ในรูปที่ 7
พลังงานที่ยึดจับคำนวณโดยวิธีพื้นที่ผิวเกิดทั่วไปของกลศาสตร์โมเลกุล (MM-GBSA) [39] พลังงานอิสระในการยึดเกาะที่คาดการณ์ไว้ของ blestrin D กับไทโรซิเนสและอะดีนิเลตไซคเลสเท่ากับ−96.94kcal/mol และ−139.69kcal/mol ตามลำดับ ซึ่งบ่งบอกว่าอันตรกิริยาการจับนั้นเกิดขึ้นเองตามธรรมชาติ (ตารางที่ 5) นอกจากนี้ การสนับสนุนที่สนับสนุนการจับลิแกนด์คือปฏิกิริยาการละลายแบบไม่มีขั้ว, van der Waals และปฏิกิริยาระหว่างไฟฟ้าสถิต

ตารางที่ 3บทสรุปของสัมพรรคภาพในการจับและอันตรกิริยาของกรดลิแกนด์-อะมิโน
การอภิปราย
เป็นที่น่าสังเกตว่าประเภทและเนื้อหาของส่วนประกอบทางเคมีใน EFB มีมากกว่า inETB พื้นที่พีคของสารประกอบที่ระบุใน EFB มีค่าประมาณสองเท่าของสารประกอบใน ETB Mili-tarine เป็นสารประกอบที่มีมากที่สุดทั้งใน EFBand ETB ซึ่งมีสารต้านอนุมูลอิสระ ต้านการอักเสบ และป้องกันระบบประสาท และได้รับเลือกให้เป็นตัวบ่งชี้ทางเคมีสำหรับการควบคุมคุณภาพของ B. striata ใน Chinese Pharmacopoeia2020 edition [46] พื้นที่พีคสัมพัทธ์ของทหารในEFB (38.39×106) สูงกว่าใน ETB(30.48×106) เล็กน้อย Gastrodin เป็นสารประกอบที่รู้จักกันดีในยาสมุนไพรจีนหลายชนิด เช่น Gastrodia elata ซึ่งแสดงฤทธิ์ยับยั้งไทโรซิเนสอย่างมีนัยสำคัญและผลการขับรังสีแคลอรี [30] พื้นที่พีคสัมพัทธ์ของ gastrodin ใน EFB (1.43 × 106) ต่ำกว่า inETB (2.17 × 106) เล็กน้อย
สารสกัดเอธานอล 95 เปอร์เซ็นต์ของ TB และ PB มีฤทธิ์ต้านออกซิเดชันในหลอดทดลองที่แข็งแกร่งกว่าสารโพลีแซค-คาไรด์แบบหยาบ นอกจากนี้ EFB ยังแสดงฤทธิ์ต้านอนุมูลอิสระที่แข็งแกร่งกว่า ETB ซึ่งสอดคล้องกับผลการวิจัยก่อนหน้านี้ [25] ปรากฏการณ์นี้อาจเกิดจากการที่ EFB มีสารประกอบต้านอนุมูลอิสระในระดับที่สูงกว่า เช่น มิลิทารีนและสติลบีนอยด์ (โพลีฟีนอลจากพืชธรรมชาติ) ตัวอย่างเช่น พื้นที่พีคสัมพัทธ์ของ 4,8,4′,8′-tetramethoxy-[1,1′-biphenanthrene]-2,7,2′,7′-tetrol, biphenanthrene with four phenolic hydroxylgroups, คือ 9.15×106 ใน FB ขณะที่เป็น 0.01×106 inTB
ในการศึกษาปัจจุบัน PPB และ PTB แสดงฤทธิ์การยับยั้งไทโรซิเนสเล็กน้อยในลักษณะที่ขึ้นกับขนาดยา อย่างไรก็ตาม แสดงให้เห็นว่าไม่มีการตรวจพบกิจกรรมในสารสกัดที่เป็นน้ำของ PB (ประกอบด้วย PPB) [25] ปรากฏการณ์นี้อาจเกิดจากการเตรียมตัวอย่างที่แตกต่างกัน สารสกัดที่เป็นน้ำของ PB ถูกใช้ในกิจกรรมการยับยั้งการประเมินไทโรซิเนสในการทดลองของ Jiang [25] ในขณะที่ในการศึกษานี้ สารสกัดที่เป็นน้ำถูกตกตะกอนด้วยเอทานอลเพื่อให้ได้พอลิแซ็กคาไรด์แบบหยาบ
เมื่อเร็ว ๆ นี้ แบบจำลองม้าลายใช้กันอย่างแพร่หลายในการประเมินฤทธิ์ต้านการสร้างเม็ดสีในร่างกาย [47, 48] Arbu-tin ซึ่งเป็นสารประกอบไฮโดรควิโนนกลูโคไซด์ที่มีอยู่ในพืชต่างชนิดกัน ซึ่งมีการใช้ในเชิงพาณิชย์ในอุตสาหกรรมเครื่องสำอาง ถูกกำหนดให้เป็นตัวควบคุมเชิงบวก ฤทธิ์ต้านการสร้างเม็ดสีของ ETB และ EFB นั้นแข็งแกร่งกว่าอาร์บูติน ซึ่งบ่งชี้ว่า ETB และ EFB สามารถนำมาใช้เป็นสารปรับผิวขาวในอุตสาหกรรมเครื่องสำอางได้
พื้นที่พีคสัมพัทธ์ของ blestrin D ใน EFB(1.91 × 106) มีค่าประมาณสี่เท่าของค่านั้นใน ETB(0.46 × 10 ) พื้นที่พีคสัมพัทธ์ของสารประกอบ 56 (8.73 × 106) และ 93 (0.64 × 106) ใน EFB ก็สูงกว่าใน ETB อย่างมีนัยสำคัญเช่นกัน (น้อยกว่า 0.01×106 และ0.10 × 106) นี่อาจเป็นสาเหตุหนึ่งที่ EFB แสดงฤทธิ์ต้านการสร้างเม็ดสีที่แข็งแรงกว่า ETB เป็นที่น่าสนใจที่จะสังเกตว่าแกนด์สามตัวที่มุ่งไปที่ไทโรซิเนสและอะเดนิเลตไซโคลสล้วนเป็นของสติลบีนอยด์ (ไบเบนซิล ฟีแนนทรีนและอนุพันธ์ของมัน) สติลบีนอยด์เป็นโพลีฟีนอลจากพืชธรรมชาติ ซึ่งดึงดูดความสนใจอย่างมากในช่วงหลายปีที่ผ่านมาเนื่องจากฤทธิ์ทางชีวภาพที่โดดเด่นของพวกมัน เช่น ฤทธิ์ต้านการอักเสบ ต้านจุลชีพ และสารต้านอนุมูลอิสระ [49] Resveratrol เป็นสทิลบีนอยด์ที่พบได้บ่อยที่สุด งานวิจัยก่อนหน้านี้ระบุว่าเรสเวอราทรอลและอนุพันธ์ของเรสเวอราทรอลสามารถยับยั้งกิจกรรมการเร่งปฏิกิริยา การแสดงออกของยีน และการปรับเปลี่ยนไทโรซิเนสภายหลังการแปลอย่างมีนัยสำคัญ ดังนั้น สารเหล่านี้จึงแสดงให้เห็นว่ามีประโยชน์ในฐานะสารปรับสภาพผิวและต่อต้านริ้วรอยในเครื่องสำอาง [41, 50]

Cistanche แสดงให้เห็นว่ามีประโยชน์ในการทำให้ผิวขาวและสารต่อต้านริ้วรอยในเครื่องสำอาง
สำหรับข้อมูลเพิ่มเติมกรุณาคลิกที่ภาพ
บทสรุป
ในการศึกษานี้ ฤทธิ์ต้านอนุมูลอิสระและฤทธิ์ต้านการสร้างเม็ดสีของพอลิแซ็กคาไรด์ดิบจาก B. striatatuber (PTB) และรากที่มีเส้นใย (FPB) และสารสกัดจากเอธานอล 95 เปอร์เซ็นต์ของ B. striata tuber (ETB) และ fibrous root (EFB) ได้รับการตรวจสอบอย่างเป็นระบบ . ผลการศึกษาพบว่า EFB มี DPPH แรงที่สุด ฤทธิ์กำจัดอนุมูลอิสระ ABTS และกิจกรรมลดธาตุเหล็กเฟอร์ริก นอกจากนี้ ETB และ EFB สามารถลดกิจกรรมของไทโรซิเนสในหลอดทดลองและการสังเคราะห์เมลานินของตัวอ่อนม้าลายในลักษณะที่ขึ้นกับขนาดยาได้อย่างมีนัยสำคัญ การเทียบท่าระดับโมเลกุลบ่งชี้ว่ามีสารประกอบจำนวนมาก ซึ่งส่วนใหญ่เป็นของสติลบีนอยด์ แสดงสัมพรรคภาพในการจับที่แรงขึ้นต่อไทโรซิเนสและอะดีนีเลตไซคเลส เมื่อเทียบกับสัมพรรคภาพการจับของลิแกนด์ดั้งเดิม การค้นพบนี้สนับสนุนเหตุผลสำหรับการใช้ ETB และ EFB เป็นสารฟอกสีผิวตามธรรมชาติในอุตสาหกรรมยาและเครื่องสำอาง
