วงจรเซลล์ประสาทและไซแนปส์แบบประหยัดพื้นที่และพลังงานที่ใช้ CMOS สำหรับเครือข่ายประสาทเทียมแบบอะนาล็อกโดเมนเวลา
Dec 06, 2023
เชิงนามธรรม
โครงสร้างประสาทแบบทั่วไปมีแนวโน้มที่จะสื่อสารผ่านปริมาณแอนะล็อก เช่น กระแสหรือแรงดันไฟฟ้า อย่างไรก็ตาม เนื่องจากอุปกรณ์ CMOS ลดขนาดลงและแรงดันไฟฟ้าของแหล่งจ่ายลดลง ช่วงไดนามิกของวงจรแอนะล็อกของโดเมนแรงดัน/กระแสจะแคบลง อัตรากำไรที่มีอยู่จะน้อยลง และภูมิคุ้มกันสัญญาณรบกวนลดลง ยิ่งไปกว่านั้น การใช้แอมพลิฟายเออร์ในการปฏิบัติงาน (ออปแอมป์) และเครื่องเปรียบเทียบเวลาต่อเนื่องหรือแบบโอเวอร์คล็อกในการออกแบบทั่วไปทำให้เกิดการใช้พลังงานสูงและพื้นที่ชิปขนาดใหญ่ ซึ่งจะเป็นอันตรายต่อการสร้างโครงข่ายประสาทเทียมที่พุ่งสูงขึ้น ด้วยเหตุนี้ เราจึงเสนอโครงสร้างประสาทสำหรับการสร้างและการส่งสัญญาณโดเมนเวลา รวมถึงโมดูลเซลล์ประสาท โมดูลไซแนปส์ และโมดูลน้ำหนักสองโมดูล โครงสร้างประสาทที่นำเสนอนั้นขับเคลื่อนโดยกระแสรั่วไหลของทรานซิสเตอร์ MOS และใช้ตัวเปรียบเทียบที่ใช้อินเวอร์เตอร์เพื่อสร้างฟังก์ชันการยิง จึงให้พลังงานและพื้นที่ที่มีประสิทธิภาพสูงกว่าเมื่อเทียบกับการออกแบบทั่วไป โครงสร้างประสาทที่นำเสนอนั้นประดิษฐ์ขึ้นโดยใช้เทคโนโลยี TSMC 65 นาโนเมตร CMOS เซลล์ประสาทและไซแนปส์ที่นำเสนอนั้นครอบครองพื้นที่ 127 และ 231 ลูกบาศก์เมตร ตามลำดับ ในขณะที่บรรลุค่าคงที่เวลามิลลิวินาที การวัดชิปตามจริงแสดงให้เห็นว่าโครงสร้างที่นำเสนอใช้ฟังก์ชันการสื่อสารสัญญาณชั่วคราวด้วยค่าคงที่เวลามิลลิวินาที ซึ่งเป็นขั้นตอนสำคัญในการประมวลผลอ่างเก็บน้ำฮาร์ดแวร์สำหรับการโต้ตอบระหว่างมนุษย์และคอมพิวเตอร์ ผลการจำลองของโครงข่ายประสาทเทียมที่พุ่งขึ้นอย่างรวดเร็วสำหรับการคำนวณอ่างเก็บน้ำด้วยแบบจำลองพฤติกรรมของโครงสร้างประสาทที่นำเสนอแสดงให้เห็นถึงฟังก์ชันการเรียนรู้

ประโยชน์ของซิสตานช์สำหรับระบบภูมิคุ้มกันของผู้ชาย
คลิกที่นี่เพื่อดูผลิตภัณฑ์ Cistanche Enhance Immunity
【สอบถามเพิ่มเติม】 อีเมล:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
โครงข่ายประสาทเทียมเชิงลึก (DNN) ซึ่งเป็นโครงข่ายประสาทเทียม (ANN) รุ่นที่สอง ได้รับการสำรวจอย่างกว้างขวางในช่วงไม่กี่ปีที่ผ่านมาสำหรับแอปพลิเคชันที่มีจำนวนเพิ่มมากขึ้น อย่างไรก็ตาม การใช้พลังงานมหาศาลโดยเฉพาะอย่างยิ่งในการเข้าถึงหน่วยความจำในสถาปัตยกรรม von Neumann แบบเดิมได้บังคับให้ผู้คนค้นหาวิธีอื่นเพื่อให้ได้โซลูชันที่ประหยัดพลังงานมากขึ้น1–6 Spiking neural network (SNN) เป็นหนึ่งในโซลูชันที่น่าสนใจเป็นอันดับสาม การสร้าง ANN ที่สามารถรับรู้ฟังก์ชันการเรียนรู้ด้วยพลังงานต่ำโดยการเลียนแบบเซลล์ประสาททางชีววิทยา SNN ประกอบด้วยเซลล์ประสาทและไซแนปส์ และมักจะสร้างขึ้นโดยใช้วิธีจากล่างขึ้นบน ซึ่งหมายความว่าแต่ละองค์ประกอบของ SNN จำเป็นต้องได้รับการออกแบบก่อน6–12 มีการรายงานการใช้งานฮาร์ดแวร์หลายอย่างของเซลล์ประสาทแบบพัลซ์หรือไซแนปส์13–21 ถึง ใช้ฟังก์ชันการรวมที่รั่วของเซลล์ประสาท การออกแบบทั่วไปมักจะสร้างผู้รวมระบบด้วยแอมพลิฟายเออร์ในการดำเนินงาน (ออปแอมป์)14 และมักใช้ตัวเก็บประจุและตัวต้านทานบนชิปขนาดใหญ่เพื่อเลียนแบบค่าคงที่เวลามิลลิวินาทีของเซลล์ประสาทชีวภาพ16,17 ยิ่งไปกว่านั้น เพื่อดำเนินการ ฟังก์ชัน "ไฟ" ของเซลล์ประสาท ซึ่งเป็นโครงสร้างวงจรเฉพาะของตัวเปรียบเทียบเวลาต่อเนื่องหรือแบบโอเวอร์คล็อกมักจะใช้เพื่อกำหนดเกณฑ์สำหรับการกระตุ้นเซลล์ประสาท 13–16,20 กระแสไบแอสของตัวเปรียบเทียบเวลาต่อเนื่องจะเพิ่มการใช้พลังงานของ ในขณะที่ตัวเปรียบเทียบแบบโอเวอร์คล็อกต้องการการกระจายสัญญาณนาฬิกาเพิ่มเติม และโครงสร้างตัวเปรียบเทียบที่ซับซ้อนนั้นครอบครองพื้นที่ชิปขนาดใหญ่ ในขณะที่กระบวนการขั้นสูงกว่าสามารถบรรลุถึงการใช้พลังงานที่ต่ำโดยการลดแรงดันแหล่งจ่ายและกระแสรั่วไหลแบบคงที่21 ยังนำไปสู่ช่วงไดนามิกที่แคบลง อัตรากำไรที่มีอยู่น้อยลง และภูมิคุ้มกันทางเสียงที่ลดลงของวงจรแอนะล็อกโดเมนแรงดัน/กระแส22 ซึ่งเป็นอันตรายต่อ โครงข่ายประสาทเทียมทั่วไปที่ใช้ปริมาณแอนะล็อก เช่น แรงดันและกระแส เพื่อสื่อสารระหว่างกัน ในทางกลับกัน ต้องขอบคุณทรานซิสเตอร์ที่ปรับขนาดซึ่งมีความเร็วการทำงานที่ดีขึ้นพร้อมการเปลี่ยนสัญญาณที่คมชัด ข้อมูลอะนาล็อกจึงสามารถแสดงได้อย่างมีประสิทธิภาพมากขึ้นในโดเมนเวลา กล่าวคือ ช่วงเวลาของการเปลี่ยนสัญญาณสองครั้ง สิ่งที่เรียกว่าวงจรโดเมนเวลานี้มีข้อได้เปรียบอีกประการหนึ่งในด้านประสิทธิภาพการใช้พลังงาน เนื่องจากมักประกอบด้วยอินเวอร์เตอร์หรือลอจิกเกตที่ไม่ใช้พลังงาน DC22,23 ดังนั้น วงจรโดเมนเวลาจึงเหมาะอย่างยิ่งสำหรับการใช้งาน SNN ที่ใช้พลังงานต่ำในอนาคต .

ประโยชน์ของซิสตานช์สำหรับระบบภูมิคุ้มกันของผู้ชาย
ในบทความนี้ เราเสนอโครงสร้างประสาทดั้งเดิมสำหรับการสร้างและการส่งสัญญาณโดเมนเวลาเพื่อสร้างเครือข่ายประสาทโดเมนเวลา โครงสร้างแบบผสมผสานประกอบด้วยโมดูลเซลล์ประสาทและไซแนปส์ที่สร้างและส่งสัญญาณโดเมนเวลาตามลำดับ รวมถึงโมดูลน้ำหนักสำหรับฟังก์ชันการเรียนรู้ แอปพลิเคชันเป้าหมายหลักประการหนึ่งของเราคือการประมวลผลอ่างเก็บน้ำ ซึ่งประมวลผลข้อมูลที่เกี่ยวข้องกับกิจกรรมของมนุษย์ แอปพลิเคชันของเรามีเป้าหมายในการประมวลผลที่ง่ายขึ้นและใช้ข้อมูลน้อยลง เช่น สัญญาณชีวภาพ ในการคำนวณอ่างเก็บน้ำ ฟังก์ชันการเรียนรู้ เช่น ECG และการจดจำผู้พูด รวมถึงการจดจำลายมือ สามารถนำมาใช้ได้โดยใช้เซลล์ประสาทเพียงไม่กี่ร้อยตัว ข้อมูลอ้างอิง 24 แสดงให้เห็นว่าประสิทธิภาพการเรียนรู้ดีขึ้นเมื่อค่าคงที่เวลาของเอฟเฟกต์อินพุตถูกจับคู่ระหว่างฟังก์ชันเป้าหมายและไดนามิกของแหล่งสำรอง และเราใช้ค่าคงที่เวลามิลลิวินาทีเป็นเป้าหมายการออกแบบสำหรับโครงสร้างประสาทที่จะใช้ในการประมวลผลข้อมูลอนุกรมเวลาของ กิจกรรมของมนุษย์ เราใช้แบบจำลองพฤติกรรมของโครงสร้างประสาทที่นำเสนอเพื่อสร้าง SNN สำหรับการประมวลผลอ่างเก็บน้ำ และใช้ฟังก์ชันการเรียนรู้ ซึ่งพิสูจน์ว่าโครงสร้างประสาทที่เรานำเสนอสามารถนำมาใช้สำหรับการประมวลผลอ่างเก็บน้ำได้ โครงสร้างประสาทที่ออกแบบและประดิษฐ์จะแสดงในรูปที่ 1(a) ซึ่งขึ้นอยู่กับโมดูลเซลล์ประสาท ไซแนปส์ และน้ำหนักที่เสนอ ซึ่งจะอธิบายในรายละเอียดด้านล่าง ในโครงสร้างนี้ ข้อมูลเข้าของโมดูลเซลล์ประสาทเชื่อมต่อกับโมดูลน้ำหนักสองโมดูล โมดูลหนึ่งสำหรับปรับสัญญาณยับยั้ง และอีกโมดูลสำหรับสัญญาณกระตุ้น เราประดิษฐ์โครงสร้างประสาทที่นำเสนอซึ่งแสดงในรูปที่ 1(a) ด้วยเทคโนโลยี CMOS มาตรฐาน TSMC 65 นาโนเมตร ภาพไมโครกราฟของชิปแสดงในรูปที่ 1(b) โดยที่พื้นที่ตายของเซลล์ประสาท ไซแนปส์ และโมดูลน้ำหนักคือ 127, 231 และ 525 lm2 ตามลำดับ
โมดูล ght คือ 127, 231 และ 525 lm2 ตามลำดับ แบบจำลองเซลล์ประสาท LIF ประกอบด้วยตัวเก็บประจุเมมเบรน ตัวต้านทานการรั่ว และเครื่องเปรียบเทียบแรงดันไฟฟ้าเป็นส่วนใหญ่ เซลล์ประสาทรับสัญญาณจากเซลล์ประสาทอื่นๆ ผ่านทางไซแนปส์ และโสมจะสร้างศักยะงานในการตอบสนองต่อสัญญาณภายนอกเหล่านี้ หากเซลล์ประสาทได้รับจำนวนเดือยที่เพียงพอผ่านทางไซแนปส์ ศักยภาพของเมมเบรนจะถึงค่าเกณฑ์ ส่งผลให้เซลล์ประสาท "ส่งสัญญาณ"8,25,26 การใช้อินเวอร์เตอร์เพื่อใช้งานฟังก์ชัน "ไฟ" เป็นที่ทราบกันดีอยู่แล้วในชื่อ ทางเลือกแทนการเปรียบเทียบ ข้อมูลอ้างอิงที่ 27 ได้เสนอเซลล์ประสาทที่ใช้อินเวอร์เตอร์ ซึ่งเหมาะอย่างยิ่งสำหรับใช้ในโครงสร้างประสาทที่เสนอ ดังนั้นเซลล์ประสาทที่ใช้ในการศึกษานี้จึงได้รับการออกแบบตามการอ้างอิง 27 ซึ่งแสดงในรูปที่ 2(a) ประกอบด้วยอุปกรณ์อินพุต อุปกรณ์รวมระบบรั่ว อุปกรณ์ดับเพลิง และอุปกรณ์หน่วงเวลา เดิมทีใน Ref. ในรูปที่ 27 วงจรไม่ถือว่าได้รับการออกแบบเป็นองค์ประกอบในการสร้างโครงข่ายประสาทเทียม ดังนั้นจึงไม่มีโครงสร้างในการรับสัญญาณกระตุ้นและยับยั้ง ในทางกลับกัน ในวงจรที่เสนอ อุปกรณ์อินพุตที่ประกอบด้วย M1 และ M2 จะได้รับอินพุตแบบกระตุ้นและอินพุตแบบยับยั้งตามลำดับ อินพุตของ M1 และ M2 เป็นสัญญาณพัลส์แคบดังแสดงในรูปที่ 2 (a) ซึ่งสร้างขึ้นจากไซแนปส์ก่อนสเตจ กิจกรรมของไซแนปส์ก่อนสเตจแสดงด้วยความถี่พัลส์ และน้ำหนักการเชื่อมต่อแสดงด้วยความกว้างพัลส์ เมื่อมีการเชื่อมต่อไซแนปส์ก่อนสเตจมากกว่าหนึ่งตัวเพื่อสร้างเครือข่าย สามารถใช้พัลส์หลายตัวผ่านตรรกะ OR หรือโดยการเพิ่มอุปกรณ์อินพุตที่เชื่อมต่อแบบขนาน ด้วยอุปกรณ์อินพุตแบบขนาน วงจรเซลล์ประสาทสามารถรับหลายพัลส์ได้ในเวลาเดียวกัน

cistanche tubulosa-ปรับปรุงระบบภูมิคุ้มกัน
ในอุปกรณ์ตัวรวมที่รั่ว Cmem แสดงถึงเยื่อหุ้มเซลล์ของเซลล์ประสาท และ M5 ถือได้ว่าเป็นตัวต้านทานที่รั่วในสถานะพัก เมื่อไม่มีอินพุตภายนอกไปยังอุปกรณ์อินพุต ตัวเก็บประจุจะถูกชาร์จด้วยกระแสรั่วไหลของ M3 และ M4 และศักยภาพของเมมเบรน Vmem จะเพิ่มขึ้นอย่างต่อเนื่องตามกระแสไหลเข้าของกระแสรั่วไหล [กระแสถูกรวมเข้าด้วยกัน ดังแสดงในรูปที่ 2( สอง)]. ณ จุดนี้ เนื่องจาก M5 อยู่ในสถานะปิด จึงถือได้ว่าเป็นตัวต้านทานแบบขนานกับตัวเก็บประจุ กล่าวคือ ตัวต้านทานรั่ว ซึ่งสามารถให้ค่าคงที่เป็นเวลานานได้ เมื่อ Vmem เพิ่มขึ้นถึงแรงดันไฟฟ้าเกณฑ์VthðFireÞ อุปกรณ์การยิงจะถูกเปิดใช้งาน [รูปที่. 2(ข-ii)]. ในการออกแบบทั่วไป เซลล์ประสาท LIF ส่วนใหญ่ใช้โครงสร้างวงจรเฉพาะของตัวเปรียบเทียบเวลาต่อเนื่องหรือแบบโอเวอร์คล็อกเพื่อตั้งค่าแรงดันไฟฟ้าที่เกณฑ์ สิ่งนี้ไม่เป็นมิตรสำหรับการสร้าง SNN ที่มีประสิทธิภาพด้านพลังงานและมีขนาดทางชีวภาพเท่ากับสมอง ในการศึกษานี้ อุปกรณ์การยิงถูกใช้งานโดยตัวเปรียบเทียบที่ใช้อินเวอร์เตอร์ ซึ่งสามารถตั้งค่าแรงดันไฟฟ้าตามเกณฑ์ด้วยทรานซิสเตอร์สองตัว แทนที่จะเป็นตัวเปรียบเทียบเวลาต่อเนื่องหรือแบบโอเวอร์คล็อก เพื่อให้ทราบถึงแรงดันไฟฟ้าเกณฑ์ที่แม่นยำสำหรับเครื่องเปรียบเทียบที่ใช้อินเวอร์เตอร์ เราอาจใช้เทคนิคการปรับศูนย์อัตโนมัติซึ่งจะตรวจจับ จัดเก็บ และยกเลิกออฟเซ็ตด้วยสวิตช์และตัวเก็บประจุเป็นระยะๆ28 อย่างไรก็ตาม ต้องใช้นาฬิกาหลายเฟสเพื่อควบคุมสวิตช์ จึงไม่เหมาะกับการใช้งานอ่างเก็บน้ำแบบประหยัดพื้นที่และพลังงาน แม้ว่าจะใช้เครื่องเปรียบเทียบแบบธรรมดาที่ใช้อินเวอร์เตอร์ แต่เกณฑ์ขั้นต่ำอาจเปลี่ยนแปลงได้เนื่องจากกระบวนการ แรงดันไฟฟ้า และความผันผวนของอุณหภูมิ แต่ก็สามารถมองว่าเป็นการเลียนแบบความแตกต่างระหว่างบุคคลในเซลล์ประสาทจริง นอกจากนี้ ฟังก์ชันการเรียนรู้สามารถชดเชยความแตกต่างของเกณฑ์และความแปรผันของกระบวนการได้29 เมื่อมีอินพุตพัลส์กระตุ้น M1 จะเปิดขึ้นทันที ซึ่งทำให้กระแสชาร์จ Cmem และ Vmem เพิ่มขึ้นอย่างรวดเร็ว ในทางกลับกัน สัญญาณอินพุตพัลส์แบบยับยั้งจะทำให้ M2 เปิดขึ้นชั่วขณะ ส่งผลให้ Cmem ชาร์จช้าลงหรือแม้กระทั่งคายประจุผ่าน M2 ซึ่งจะทำให้อัตรา Vmem เพิ่มขึ้นหรือลดลงช้าลง
เมื่ออุปกรณ์การยิงถูกเปิดใช้งาน มันจะสร้าง VFire ระดับต่ำเพื่อเชื่อมต่อกับ M4 ซึ่งจะเพิ่มกระแสเพื่อชาร์จตัวเก็บประจุเมมเบรน Cmem ส่งผลให้ Vmem ที่มีศักยภาพของเมมเบรนเพิ่มขึ้นทันที ซึ่งส่งเสริมการกระตุ้นการยิง อุปกรณ์. สิ่งนี้เลียนแบบการไหลเข้าของ Naþ เข้าสู่เยื่อหุ้มเซลล์ กระตุ้นให้แรงดันไฟฟ้าของเมมเบรนเพิ่มขึ้นอย่างรวดเร็ว กล่าวคือ ผลตอบรับเชิงบวก ในที่สุด VFire ระดับต่ำที่สร้างขึ้นจากอุปกรณ์ยิงจะถูกแปลงเป็น VSpike ในระดับสูง [รูปที่ 1] 2(b-iii)] โดยอุปกรณ์หน่วงเวลาที่มีอินเวอร์เตอร์สามสเตจ และเชื่อมต่อ VSpike กับ M3 และ M5 เพื่อรีเซ็ต Vmem ให้เป็นศูนย์ กระบวนการนี้เลียนแบบการกระตุ้นช่อง Kþ ในเซลล์ประสาทชีวภาพ ส่งผลให้ไอออน Kþ ไหลออก และในที่สุดเยื่อหุ้มเซลล์กลับคืนสู่สถานะพัก
ไซแนปส์เป็นโมดูลสำคัญใน SNN เนื่องจากเซลล์ประสาทเชื่อมต่อถึงกัน เราได้ออกแบบโมดูลเซลล์ประสาทสำหรับสร้างสัญญาณโดเมนเวลา จากนั้นเราจำเป็นต้องมีตัวกลางในการส่งผ่าน เช่น ไซแนปส์ เพื่อส่งสัญญาณโดเมนเวลานี้ไปยังเซลล์ประสาทอื่นๆ ในการสร้างโครงข่ายประสาทเทียมที่สมบูรณ์ เราได้ออกแบบโมดูลไซแนปส์ตามสัญญาณความถี่ ดังแสดงในรูปที่ 2(c) ไซแนปส์ส่วนใหญ่ประกอบด้วยวงแหวนออสซิลเลเตอร์ควบคุมแรงดันไฟฟ้าที่ทำงานภายใต้กระแสรั่วไหล ซึ่งประกอบด้วยอินเวอร์เตอร์สามขั้นตอน (M6; M7; M8; M9; M10 และ M11) วงจรเซลล์ประสาทก่อนหน้านี้จะยิงและสร้าง VSpike ที่ขัดขวางซึ่งอินเวอร์เตอร์กลับด้าน ทำให้ M5 เปิดในช่วงเวลาสั้นๆ และกระแสที่ไหลผ่าน M5 จะชาร์จ CSYN ซึ่งจะเพิ่ม VSYN เมื่อ VSYN ถึงแรงดันไฟฟ้าที่ทำให้เกิดการสั่น ริงออสซิลเลเตอร์จะเริ่มสั่น [รูปที่. 2(b-iv) และ 2(bv)] หากเซลล์ประสาทที่อยู่ก่อนหน้าไม่ทำงานเป็นเวลานาน VSYN จะรั่วไหลจนกระทั่งถึงสถานะเริ่มต้น ซึ่ง ณ จุดนี้ไซแนปส์จะไม่ทำงานอีกครั้ง เนื่องจาก VSYN เทียบเท่ากับแรงดันแหล่งจ่ายของริงออสซิลเลเตอร์ กระแสที่ไหลออกจาก M5 จะควบคุม VSYN และด้วยเหตุนี้ ความถี่ของริงออสซิลเลเตอร์

ประโยชน์ของซิสตานช์สำหรับระบบภูมิคุ้มกันของผู้ชาย
SNN บรรลุฟังก์ชันการเรียนรู้โดยการปรับน้ำหนัก ดังนั้นเราจึงเสนอโมดูลน้ำหนักที่เข้ากันได้กับเซลล์ประสาทโดเมนเวลาที่เสนอและโมดูลไซแนปส์ที่อธิบายไว้ข้างต้น ดังแสดงในรูปที่ 2(d) โมดูลน้ำหนักที่นำเสนอจะปรับข้อมูลโดเมนเวลา ซึ่งเป็นความกว้างของพัลส์เอาท์พุต โมดูลนี้ประกอบด้วยเส้นหน่วงเวลา มัลติเพล็กเซอร์ และเกท AND VRing คือสัญญาณคลื่นสี่เหลี่ยมจากไซแนปส์ที่จะผ่านเส้นหน่วงเวลา VWeight คือรหัสดิจิทัลที่แสดงถึงน้ำหนัก ซึ่งจะถูกกำหนดหลังจากการเรียนรู้และใช้ในการควบคุมมัลติเพล็กเซอร์ ความกว้างของพัลส์เอาท์พุตที่สอดคล้องกับน้ำหนักโดเมนเวลาจะถูกปรับตามการต๊าปในวงจรอินเวอร์เตอร์ที่เลือกโดยมัลติเพล็กเซอร์ ตามที่กล่าวไว้ข้างต้น ถ้าความกว้างของพัลส์ที่ถูกกระตุ้นหรือยับยั้งกว้าง แรงดันไฟฟ้า Vmem ในเซลล์ประสาทถัดไปจะถูกชาร์จหรือคายประจุเร็วขึ้นตามลำดับ ซึ่งสอดคล้องกับน้ำหนักที่มาก ในการศึกษานี้ เราเลือกมัลติเพล็กเซอร์ที่มีอินพุต 16 ตัว เช่น น้ำหนักสี่บิต (0000 ถึง 1111) เอาต์พุตของโมดูลน้ำหนักเชื่อมต่อกับอุปกรณ์อินพุตของวงจรเซลล์ประสาทที่ตามมา ความถี่ของพัลส์ (ระยะห่างระหว่างพัลส์) และความกว้างของพัลส์ทำหน้าที่พร้อมกันบนเซลล์ประสาทเพื่อเปลี่ยนกิจกรรมของมัน ความถี่ของพัลส์ถูกกำหนดโดยความถี่เอาต์พุตของไซแนปส์ก่อนหน้า ในขณะที่ความแรงของการเชื่อมต่อจะขึ้นอยู่กับความกว้างของเอาต์พุตพัลส์ที่กำหนดโดยโมดูลน้ำหนัก
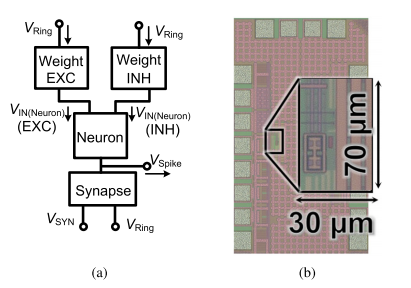
รูปที่. 1. (a) โครงสร้างที่เสนอและ (b) ไมโครกราฟของชิป

รูปที่. 2. (a) แผนภาพวงจรของโมดูลเซลล์ประสาทที่เสนอ (b) พฤติกรรมของเซลล์ประสาท LIF และโมดูลไซแนปส์ที่เสนอ (c) แผนภาพวงจรของโมดูลไซแนปส์ที่เสนอ และ (d) แผนภาพวงจรของโมดูลน้ำหนักที่เสนอ
รูปที่ 3(a) แสดงการตั้งค่าการทดลองที่ใช้ในการทดสอบชิปโครงสร้างประสาทที่ประดิษฐ์ขึ้น ตามมาตรา 1(b)] โดยวางชิปไว้บนสถานีโพรบ Summit 11000 และทดสอบด้วยโพรบที่สัมผัสโดยตรงกับชิป ในการทดลอง เราถือว่าอินพุตของโมดูลน้ำหนักทั้งสองเป็นไซแนปส์ก่อนสเตจ ซึ่งจำลองโดยตัวสร้างฟังก์ชันที่กำหนดเอง เอาต์พุตของเซลล์ประสาทเชื่อมต่อกับโมดูลไซแนปส์ ซึ่งเอาต์พุตจะแปรผันตามการเปลี่ยนแปลงในเอาต์พุตของเซลล์ประสาท เราใช้เครื่องกำเนิดฟังก์ชันตามอำเภอใจของ Tektronix AFG31252 เป็นไซแนปส์ก่อนขั้นตอนเพื่อจัดเตรียมสัญญาณคลื่นสี่เหลี่ยมสำหรับวงจรประสาทที่ประดิษฐ์ขึ้นของเรา ในเวลาเดียวกัน เราสังเกตรูปคลื่นเอาท์พุตโดยใช้ออสซิลโลสโคป (Keysight MSOX6004A และ DSOX93304Q) ผลการทดลองแสดงไว้ในรูปที่ 3(ข)–3(ง) เพื่อตรวจสอบผลกระทบของน้ำหนักต่ออัตราการยิงของเซลล์ประสาท เราได้แก้ไขความถี่ของเอาท์พุตไซแนปส์ก่อนระยะ (ตัวสร้างฟังก์ชัน) ที่ 100 Hz และสังเกตการเปลี่ยนแปลงของอัตราการยิงของเซลล์ประสาทสำหรับชิปสี่ตัวโดยการปรับโมดูลน้ำหนัก เราเฉลี่ยความถี่ขัดขวาง 1, 024 ครั้งในช่วงเวลา 100 มิลลิวินาทีเพื่อให้ได้ความถี่การยิงของเซลล์ประสาทที่สอดคล้องกันภายใต้การตั้งค่าน้ำหนักแต่ละครั้ง ดังแสดงในรูปที่ 3 (b) โดยทั่วไปแล้วเซลล์ประสาทที่นำเสนอจะยิงด้วยอัตราที่กำหนดโดยกระแสรั่วไหลเข้าและออกจาก Cmem อย่างสมดุล และอินพุตจากขั้นตอนก่อนหน้าจะปรับเซลล์ประสาท เราจะเห็นได้ว่าเมื่อน้ำหนักมากขึ้น ความถี่ในการยิงโมดูลเซลล์ประสาทก็จะมากขึ้น สาเหตุหลักมาจากความแปรผันของกระบวนการของ FET ความถี่การยิงจึงผันผวนจากประมาณ 610%–17% บนชิปสี่ตัว โดยเฉพาะอย่างยิ่งสำหรับการใช้งานในอ่างเก็บน้ำ เนื่องจากน้ำหนักแบบสุ่มในการเชื่อมต่อที่เกิดซ้ำ จึงควรชดเชยความแปรผันแบบสุ่มเหล่านี้ในระหว่างกระบวนการเรียนรู้ในน้ำหนักเอาต์พุต
รูปที่ 3 (c) เปรียบเทียบความแปรผันของเวลาการยิงของเซลล์ประสาท ขึ้นอยู่กับสัญญาณจากไซแนปส์ก่อนระยะ สิ่งที่ใส่เข้าไป (i)–(iii) ของรูปที่ 3(c) แสดงกรณีที่มีอินพุตยับยั้ง 100 Hz (น้ำหนักตั้งไว้ที่ 1100) ไม่มีอินพุต และมีอินพุตกระตุ้น 100 Hz (น้ำหนักตั้งไว้ที่ 1100) ตามลำดับ ซึ่งเราจะเห็นได้ว่าข้อมูลเข้าแบบยับยั้งจะลดความถี่ในการยิงของเซลล์ประสาท และเพิ่มช่วงการยิง ในขณะที่ข้อมูลเข้าแบบกระตุ้นจะทำงานตรงกันข้ามกับข้อมูลเข้าแบบยับยั้ง ผลการทดลองแสดงให้เห็นว่าช่วงเวลาการยิงของเซลล์ประสาทที่เสนอนั้นอยู่ในลำดับมิลลิวินาที ซึ่งสอดคล้องกับคุณลักษณะของเซลล์ประสาททางชีววิทยาที่มีค่าคงที่เวลาเป็นมิลลิวินาที เมื่อไม่มีการป้อนสัญญาณจากไซแนปส์ก่อนสเตจ ปริมาณการใช้พลังงานจะอยู่ที่ประมาณ 800 pW ซึ่งสร้างสไปค์ประมาณ 20 สไปค์ในรอบ 100 มิลลิวินาที จากนี้ สามารถประมาณได้คร่าวๆ ว่าแต่ละหนามจะใช้พลังงานประมาณ 4 pJ ต่อจากนั้นสิ่งที่ใส่เข้าไป (i) – (iii) ของรูปที่ 3 (c) ถูกนำมาใช้เป็นสัญญาณอินพุตไปยังไซแนปส์เพื่อมีอิทธิพลต่อ VRing รูปคลื่น VRing ที่วัดได้ในกรณีทั้งสามนี้จะแสดงอยู่ในรูปที่ 3(d) ค่าเฉลี่ยของความถี่สำหรับแต่ละกรณีที่วัดในช่วงเวลา 5 วินาทีคือ 41, 90 และ 98 Hz ตามลำดับ ความเป็นไปได้ของช่วงความถี่เอาต์พุตไซแนปส์นี้จะได้รับการตรวจสอบด้วยการจำลองระดับระบบในการสนทนาต่อไปนี้

รูปที่. 3. (a) ภาพถ่ายของการตั้งค่าการทดลอง (b) อัตราการยิงที่วัดได้ของเซลล์ประสาทสำหรับชิปสี่ตัว (c) รูปคลื่นที่วัดได้ของเอาต์พุตของเซลล์ประสาท และ (d) รูปคลื่นที่วัดได้ของเอาต์พุตไซแนปส์

รูปที่. 4. (a) โครงสร้างรวมอีกโครงสร้างหนึ่งที่ประดิษฐ์ขึ้นเพื่อประเมินไซแนปส์และ (b) รูปคลื่นที่วัดได้ของ VRing และ VSYN
เพื่ออำนวยความสะดวกในการสังเกตการตอบสนองแบบซิงโครนัสของไซแนปส์ เรายังสร้างโครงสร้างของรูปที่ 4(a) รูปที่ 4(b) คือผลการทดลองของรูปที่ 4(a) เราใช้เครื่องกำเนิดฟังก์ชันตามอำเภอใจของ Tektronix AFG31252 เพื่อสร้าง VIN สัญญาณคลื่นสี่เหลี่ยม 10 Hz ดังแสดงในรูปที่ 4 (ai) หลังจากที่ VIN ผ่านโมดูลน้ำหนัก มันจะสร้างสัญญาณขัดขวาง VOUTðWeightÞ แรงดันไฟฟ้า VSYN ถูกสังเกตผ่านผู้ติดตามแหล่งที่มาบนชิปเป็นบัฟเฟอร์แบบอะนาล็อก แม้ว่า VOUTðWeightÞ จะไม่ได้รับการออกแบบมาให้สังเกตจากภายนอกเนื่องจากเป็นพัลส์แคบ แต่เมื่อ VOUTðWeightÞ มาถึงหลังจากขอบตกของ VIN แรงดันไฟฟ้า VSYN ที่ไซแนปส์จะเพิ่มขึ้นทันทีดังแสดงในรูปที่ 4(b-ii) ซึ่งจะเพิ่มความถี่ของ VRing หากVOUTðWeightÞไม่ถึงเป็นเวลานาน VSYN จะลดลง ซึ่งจะส่งผลต่อความถี่ VRing ให้น้อยลง ตารางที่ 1 แสดงการเปรียบเทียบประสิทธิภาพระหว่างวงจรเซลล์ประสาทแบบสแตนด์อโลน วงจรเซลล์ประสาทที่เสนอมีข้อดีในแง่ของการใช้พลังงานและพื้นที่ การออกแบบใน Refs. 13–16 ใช้เวลาต่อเนื่องหรือตัวเปรียบเทียบแบบโอเวอร์คล็อก และการออกแบบเหล่านี้ใช้พื้นที่ชิปจำนวนมากรวมทั้งการใช้พลังงานด้วย เซลล์ประสาทที่ถูกประดิษฐ์ขึ้นในกระบวนการที่ไม่ใช่ CMOS ที่เสนอในการอ้างอิง 18 ไม่ต้องใช้เครื่องเปรียบเทียบซึ่งนำไปสู่ความได้เปรียบในพื้นที่ อย่างไรก็ตาม การใช้พลังงานค่อนข้างสูง และเทคโนโลยีเฉพาะเหล่านี้มีอายุน้อยกว่า จึงมีต้นทุนสูงกว่าเมื่อเทียบกับกระบวนการ CMOS มาตรฐาน ผู้อ้างอิงทั้งสอง หมายเลข 19 และ 21 กำลังถูกประดิษฐ์ขึ้นด้วยกระบวนการขั้นสูง อย่างไรก็ตาม เมื่อเปรียบเทียบกับงานนี้ Ref. 19 ไม่มีข้อได้เปรียบในเรื่องการใช้พลังงานและพื้นที่ แม้ว่าการอ้างอิง รูปที่ 21 แสดงประสิทธิภาพการใช้พลังงานที่ดีขึ้นพร้อมผลการจำลอง เมื่อทำให้โหนดเทคโนโลยีเป็นมาตรฐาน เซลล์ประสาทที่นำเสนอจะได้รับประสิทธิภาพของพื้นที่ที่ดีขึ้น
เพื่อแสดงให้เห็นถึงความเป็นไปได้ของเซลล์ประสาทที่หนามแหลมที่นำเสนอและวงจรไซแนปส์ที่ใช้ริงออสซิลเลเตอร์ การจำลองพฤติกรรมจะดำเนินการในสภาพแวดล้อม MATLAB ดังแสดงในรูปที่ 5(a) ในการจำลองนี้ มีการใช้เซลล์ประสาท 100 ตัวกับการเชื่อมต่อที่เกิดซ้ำแบบสุ่มกับโมดูลไซแนปส์และการถ่วงน้ำหนักที่นำเสนอ โมดูลน้ำหนักที่นำเสนอจะใช้เฉพาะในชั้นกักเก็บเท่านั้น และน้ำหนักของโมดูลดังกล่าวจะได้รับการสุ่มล่วงหน้าและคงที่ในระหว่างกระบวนการเรียนรู้ ดังนั้น ความผันผวนแบบสุ่มในแหล่งกักเก็บจะได้รับการชดเชยในระหว่างกระบวนการเรียนรู้ในน้ำหนักเอาต์พุต เพื่อสร้างการจำลองที่สมจริง ช่วงความถี่เอาต์พุตของแต่ละไซแนปส์จะถูกตั้งค่าตั้งแต่ 15 ถึง 200 Hz ตามผลการวัดจริง อัลกอริธึมกำลังสองน้อยที่สุดแบบเรียกซ้ำ (RLS) ใช้เพื่อฝึกน้ำหนักเอาต์พุตตามที่แนะนำในการอ้างอิง 30. คลื่นไซน์ 10 Hz ซึ่งสอดคล้องกับช่วงเวลาของข้อมูลที่เกี่ยวข้องกับกิจกรรมของมนุษย์ ถูกใช้เป็นตัวอย่างของสัญญาณอินพุตการควบคุมดูแล การควบคุมดูแลและสัญญาณเอาท์พุตที่ได้รับการฝึกอบรมจะแสดงในรูปที่ 5(bi) สัญญาณป้อนกลับจากเอาท์พุตจะถูกแปลงเป็นพัลส์เทรนแบบกระตุ้นและแบบยับยั้งซึ่งมีความถี่เป็นสัดส่วนกับค่าสัมบูรณ์ของแอมพลิจูดเอาท์พุตดังแสดงในรูป 5(b-ii) และ 5(b-iii) ตามลำดับ หลังจากสัญญาณการควบคุมดูแลผ่านไปห้าช่วง น้ำหนักเอาต์พุตจะคงที่ และ SNN จะสร้างสัญญาณที่เรียนรู้ด้วยตัวเอง ซึ่งแสดงให้เห็นถึงความเป็นไปได้ของโครงสร้างประสาทที่นำเสนอสำหรับฟังก์ชันการเรียนรู้ นอกจากนี้เรายังพบจากการจำลองเหล่านี้ด้วยว่าเพื่อปรับปรุงความสามารถในการเรียนรู้ให้ดียิ่งขึ้น ควรเพิ่มช่วงการปรับความถี่เอาต์พุตของไซแนปส์ ซึ่งสามารถทำได้โดยการปรับวงจรไซแนปส์ให้เหมาะสม ตัวอย่างเช่น ด้วยช่วงการปรับความถี่ที่ขยายตั้งแต่ 15 Hz–2 kHz และ 15 Hz–20 kHz สัญญาณที่เรียนรู้จะราบรื่นขึ้นเพื่อสร้างสัญญาณการตรวจสอบที่ดีขึ้นตามที่แสดงในรูปที่ 5(b-iv) และ 5(bv) ตามลำดับ

cistanche tubulosa-ปรับปรุงระบบภูมิคุ้มกัน
โดยสรุป เราได้เสนอโครงสร้างประสาทสำหรับการสร้างและส่งสัญญาณโดเมนเวลา เซลล์ประสาทและไซแนปส์ที่นำเสนอนั้นครอบครองพื้นที่ 127 และ 231 ลูกบาศก์เมตร ตามลำดับ โครงสร้างนี้ไม่ใช้ออปแอมป์และตัวเปรียบเทียบเวลาต่อเนื่องหรือแบบโอเวอร์คล็อก ในขณะที่ฟังก์ชันการยิงทำได้โดยใช้ตัวเปรียบเทียบที่ใช้อินเวอร์เตอร์เพื่อให้ข้อได้เปรียบในพื้นที่และการใช้พลังงาน โครงสร้างประสาทโดเมนเวลาที่เสนอจะได้รับประโยชน์จากเทคโนโลยีกระบวนการที่ปรับขนาดได้ เมื่อเปรียบเทียบกับการออกแบบโดเมนแรงดัน/กระแสทั่วไป ผลการวัดและการผลิตชิปที่เกิดขึ้นจริงแสดงให้เห็นถึงฟังก์ชันการสื่อสารสัญญาณชั่วคราวที่มีค่าคงที่เวลาเป็นมิลลิวินาที โครงสร้างนิวรัลโดเมนเวลาที่เสนอนั้นเหมาะอย่างยิ่งสำหรับการสร้างเครือข่ายนิวรัลที่ขัดขวางเพื่อประมวลผลข้อมูลอนุกรมเวลาแบบเรียลไทม์สำหรับการโต้ตอบระหว่างมนุษย์กับคอมพิวเตอร์
ตารางที่ 1 การเปรียบเทียบประสิทธิภาพของวงจรเซลล์ประสาทแบบสแตนด์อโลน


รูปที่. 5. (a) แบบจำลองพฤติกรรมของ SNN สำหรับการคำนวณอ่างเก็บน้ำนั้นขึ้นอยู่กับโครงสร้างประสาทที่เสนอ (b) ผลลัพธ์การจำลองพฤติกรรมระดับระบบ: (i) ขึ้นอยู่กับแบบจำลองที่มีช่วงการปรับความถี่ 15–200 Hz มุมมองแบบซูมเข้าของ (ii) การกระตุ้นและ (iii) สัญญาณอินพุตยับยั้งที่แปลงจากเอาต์พุต (iv) อิงตามช่วงการปรับความถี่ 15–2 kHz และ (v) 15–20 kHz
ข้อมูลอ้างอิง
1 Y. Zhang, P. Qu, Y. Ji, W. Zhang, G. Gao, G. Wang, S. Song, G. Li, W. Chen, W. Zheng, F. Chen, J. Pei, R Zhao, M. Zhao และ L. Shi, ธรรมชาติ 586, 378–384 (2020)
2 ดี. ชิน และ เอช.-เจ. ยู, โปรค. IEEE 108, 1245–1260 (2020)
3 วาย. เลอคุน, วาย. เบงจิโอ และจี. ฮินตัน, เนเจอร์ 521, 436–444 (2015)
4 T. Kohno และ K. Aihara, AIP Conf. โปรค 1028, 113–128 (2008)
5 อี. ชิกก้า และ ก. อินดิเวรี, Appl. ฟิสิกส์ เล็ตต์ 116, 120501 (2020)
6 Y. Bo, P. Zhang, Y. Zhang, J. Song, S. Li และ X. Liu, J. Appl. ฟิสิกส์ 127, 245101 (2020).
7 ก. ยาง และ อ. เส็งคุปตะ, Appl. ฟิสิกส์ เล็ตต์ 116, 043701 (2020)
8 X. Chen, T. Yajima, IH Inoue และ T. Iizuka, Jpn เจ. แอพพลิเคชั่น ฟิสิกส์ 61, SC1051 (2022)
9 W. Maass, ประสาท เครือข่าย 10, 1659–1671 (1997)
10ส. เอส. ราดากฤษนัน, เอ. เซบาสเตียน, เอ. โอเบรอย, เอส. ดาส และเอส. ดาส, แนท. ชุมชน 12/2143 (2021)
11X. Chen, T. Yajima, IH Inoue และ T. Iizuka ในบทคัดย่อเพิ่มเติมของการประชุมนานาชาติว่าด้วยอุปกรณ์และวัสดุโซลิดสเตต (SSDM) (JSAP, 2021), หน้า 682–683
12D. เอส.จอง,เจ.แอปพลิ. ฟิสิกส์ 124, 152002 (2018)
13ก. Indiveri, E. Chicca และ R. Douglas, IEEE Trans ประสาท เครือข่าย 17, 211–221 (2549)
14X. Wu, V. Saxena, K. Zhu และ S. Balagopal, IEEE Trans ระบบวงจร II 62, 1088–1092 (2015)
15เอ Joubert, B. Belhadj, O. Temam และ R. Heliot ในการประชุมร่วมระหว่างประเทศเรื่องโครงข่ายประสาทเทียม (IJCNN) ปี 2012
16ส. A. Aamir, P. M€uller, G. Kiene, L. Kriener, Y. Stradmann, A. Gr€ubl, J. Schemmel และ K. Meier, IEEE Trans ชีวการแพทย์ ระบบวงจร 12 ก.ค. 1027–1037 (2018)
17ก. บาซู และ พีอี ฮาสเลอร์, IEEE Trans ระบบวงจร ฉัน 57, 2938–2947 (2010)
18ส. Dutta, V. Kumar, A. Shukla, NR Mohapatra และ U. Ganguly, Sci ตัวแทน 7, 8257 (2017)
19ก. Rubino, M. Payvand และ G. Indiveri ในการประชุมนานาชาติ IEEE ว่าด้วยอิเล็กทรอนิกส์ วงจร และระบบ (ICECS) ครั้งที่ 26 (IEEE, 2019), หน้า 458–461
20ส. A. Aamir, Y. Stradmann, P. M€uller, C. Pehle, A. Hartel, A. Gr€ubl, J. Schemmel และ K. Meier, IEEE Trans ระบบวงจร ฉัน 65, 4299–4312 (2018)
21ร. M. Saber Moradi และ SA Bhave ใน IEEE Symposium Series on Computational Intelligence (SSCI) ปี 2017
22K. Asada, T. Nakura, T. Iizuka และ M. Ikeda, IEICE Electron ด่วน 15, 20182001 (2018)
23ร. Staszewski, K. Muhammad, D. Leipold, C.-M. ฮุง, วาย.-ซี. โฮ, เจ. วอลล์เบิร์ก, ซี. เฟอร์นันโด, เค. มักจิโอ, อาร์. สตาซิวสกี้, ที. จุง, เจ. โคห์, เอส. จอห์น, ไอวาย เดง, วี. ซาร์ดา, โอ. โมไรรา-ทามาโย, วี. มาเยกา, อาร์. แคทซ์ , O. Friedman, O. Eliezer, E. de Obaldia และ P. Balsara, IEEE J. Solid-State Circuits 39, 2278–2291 (2004)
24ซ. Gallicchio และ A. Micheli, ประสาท เครือข่าย 24, 440–456 (2011)
25ล. F. Abbott และ P. Dayan, ประสาทวิทยาศาสตร์เชิงทฤษฎี (The MIT Press, 2005)
26W. Gerstner และ WM Kistler, Spiking Neuron Models: Single Neurons, Populations (สำนักพิมพ์มหาวิทยาลัยเคมบริดจ์, 2012)
27ต. ยาจิมะ, วิทย์. ตัวแทน 12, 1150 (2022)
28B. Razavi, หลักการออกแบบระบบการแปลงข้อมูล (Wiley-IEEE Press, 1995)
29ต. วุนเดอร์ลิช, AF Kungl, E. M€uller, A. Hartel, Y. Stradmann, SA Aamir, A. Gr€ubl, A. Heimbrecht, K. Schreiber, D. St€ockel, C. Pehle, S. Billaudelle, G. Kiene, C. Mauch, J. Schemmel, K. Meier และ MA Petrovici จาก Front โรคประสาท 13, 1–15 (2019)
30D. Sussillo และ L. Abbott, "การสร้างรูปแบบกิจกรรมที่สอดคล้องกันจากโครงข่ายประสาทเทียมที่วุ่นวาย" Neuron 63, 544–557 (2009)
